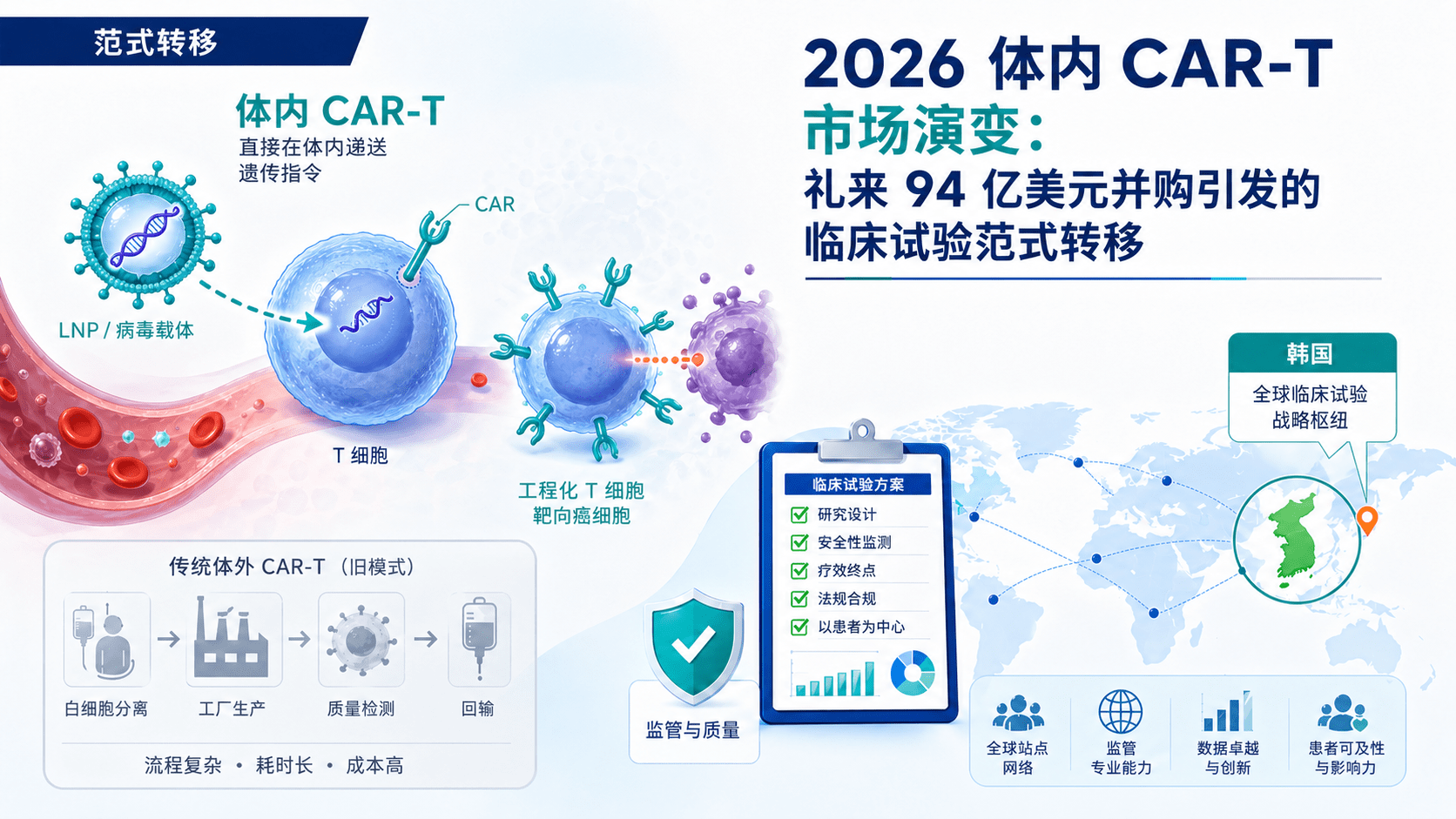
在过去十年中,嵌合抗原受体T细胞(CAR-T)疗法从根本上改变了肿瘤学格局,在难治性血液肿瘤患者中实现了前所未有的完全缓解率。然而,传统的体外(ex vivo)制造模式存在严重的结构性局限。这一过程需要通过白细胞分离术采集患者的T细胞,将其运输到集中的GMP设施,通过基因工程使其表达CAR,扩增细胞群体,最后再回输到患者体内。这种多步骤的工作流程产生了长达数周的“血管到血管”(vein-to-vein)时间,在此期间,疾病进展迅速的患者可能在接受治疗前就已去世。此外,高昂的销售成本(COGS)以及对严苛的淋巴耗竭预处理化疗的严格要求,严重制约了这些救命疗法的全球可扩展性。
截至2026年,随着“体内(in vivo)CAR-T”技术的快速临床转化,生物制药行业正在经历一场巨大的范式转变。通过利用靶向脂质纳米颗粒(LNPs)或工程化病毒载体直接进行静脉注射,体内CAR-T疗法完全绕过了体外制造的瓶颈,直接在患者体内重新编程内源性T细胞。这种从高度定制化、个体化的细胞制造服务向通用型、可扩展药物产品的转变,从根本上改变了治疗风险特征。因此,行业见证了重新设计现代临床试验协议和框架的迫切需求。本综合报告分析了主要制药公司的激进并购趋势、临床试验方案设计中出现的新挑战、美国FDA推出的最新监管灵活性,以及将韩国定位为执行全球先进临床试验首选目的地的地缘政治转变。
体内T细胞工程的科学基础与平台分类
体内CAR-T疗法的临床可行性完全取决于基因递送载体的精确度和靶向效率。载荷必须安全地绕过先天免疫系统,避免在肝脏等非靶向器官中积聚,并专门转导靶向T细胞群。目前,进入人体临床试验的递送平台大致分为两类:病毒载体和非病毒载体。
病毒载体平台:慢病毒与iGPS技术
慢病毒载体因其高转导效率和将遗传物质稳定整合到宿主基因组中的能力,长期以来一直是体外CAR-T工程的金标准。然而,传统慢病毒的全身给药存在脱靶转导和插入突变的风险。
为了解决这一问题,像Kelonia Therapeutics这样的公司开发了先进的体内基因定位系统(iGPS®)。通过修改病毒包膜糖蛋白以消除自然嗜性,并加入特定的靶向配体(如抗CD8抗体),这些工程化载体能选择性地结合并转导血液中的T细胞。由于病毒载体促进了永久性的基因组整合,该平台提供了高度持久和持续的CAR表达,使其非常适合针对复发/难治性多发性骨髓瘤等侵袭性恶性肿瘤的癌症临床试验。
非病毒载体平台:LNP与circRNA技术
相反,脂质纳米颗粒(LNP)技术代表了一种非病毒、非整合的体内T细胞工程方法。Orna Therapeutics等领先创新者利用包裹在专用LNP中的专利环状RNA(circRNA)来传递CAR遗传密码。
与线性mRNA不同,circRNA表现出卓越的细胞内稳定性和更长时间的高水平蛋白质表达。由于该平台依赖于瞬时游离体表达而非永久性基因组整合,生成的CAR-T细胞会在几周后自然衰减。这种瞬时治疗窗口对于自身免疫性疾病的临床试验(如系统性红斑狼疮SLE)非常有利,其临床目标是通过清除致病性B细胞实现临时的“免疫重置”,而非终身的CAR-T持久性。
| 评估指标 | 传统体外CAR-T | 病毒体内CAR-T(如慢病毒) | 非病毒体内CAR-T(如LNP/circRNA) |
| 制造模式 | 分散或集中的患者特定制造 | 批量生产、可扩展的通用药物 | 批量生产、可扩展的通用药物 |
| 治疗时间线 | 3至6周(从采集到回输) | 立即(静脉注射) | 立即(静脉注射) |
| 淋巴耗竭 | 植入所必需 | 通常不需要 | 不需要 |
| 表达特征 | 永久(基因组整合) | 永久(基因组整合) | 瞬时(细胞质翻译,数周内衰减) |
| 临床试验风险 | 严重的CRS、ICANS、制造失败 | 插入突变、ADA产生 | 非靶向器官积累(肝脏)、重复给药ADA |
| 目标适应症 | 血液恶性肿瘤 | 血液肿瘤和实体瘤 | 自身免疫性疾病(免疫重置)和肿瘤 |
2026年大药企并购趋势:礼来公司的全面管线扩张
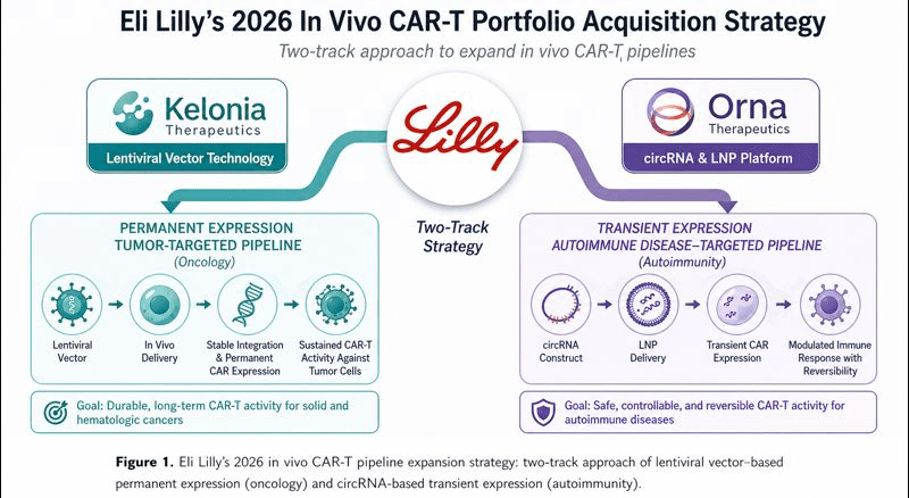
随着体内CAR-T平台成功从临床前概念验证过渡到活跃的人体临床试验,跨国制药公司已发起一波极具侵略性的并购浪潮,以确保下一代技术能力。凭借其GLP-1代谢类药物带来的前所未有的现金流,礼来公司在2026年成为主导力量,执行了两次里程碑式的收购,巩固了其在基因药物领域的领导地位。
Kelonia Therapeutics:70亿美元的收购
2026年4月,礼来公司宣布达成最终协议,以高达70亿美元的价格收购Kelonia Therapeutics,其中包括32.5亿美元的首付款和37.5亿美元的后续里程碑付款。Kelonia的核心资产KLN-1010是一款首创(first-in-class)体内CAR-T疗法,目前正处于治疗复发/难治性多发性骨髓瘤的I期临床试验中。
早期临床数据表现优异。在不进行任何淋巴耗竭预处理化疗的情况下,通过单次静脉输注,KLN-1010成功实现了强大的体内CAR-T扩增。初始队列显示出100%的微小残留病(MRD)阴性反应率,并伴有高度良好的安全性,未出现严重细胞因子释放综合征(CRS)或神经毒性。此次收购使礼来获得了一个经过验证的、能够主导未来癌症临床试验的病毒平台。
Orna Therapeutics:24亿美元的收购
为了平衡其永久表达的肿瘤组合与针对免疫学量身定制的瞬时表达平台,礼来还于2026年2月以24亿美元收购了Orna Therapeutics。Orna的领先候选药物ORN-252是一款针对CD19的体内CAR-T疗法,旨在清除导致疾病的B细胞。
随着ORN-252进入自身免疫性疾病的I期临床试验,礼来的免疫学负责人强调,体外细胞疗法的天价成本和复杂物流是更广泛自身免疫患者群体无法逾越的障碍。Orna的circRNA/LNP平台优雅地解决了这一挑战,使礼来能够在全球范围内积极扩张其自身免疫临床试验版图。
行业连锁反应与管线加速
礼来并非孤军奋战。整个行业见证了艾伯维以21亿美元收购Capstan Therapeutics,百时美施贵宝以15亿美元吸收Orbital Therapeutics,以及吉利德/Kite收购Interius BioTherapeutics。随着这些大型药企整合这些平台,全球临床试验生态系统正准备迎接大量高度复杂的、针对罕见病和常见病的基因工程疗法。
下一代临床试验方案设计的挑战与策略
将基因递送载体直接注入患者血液以在原位制造活体细胞药物,完全颠覆了传统的药代动力学(PK)和药效学(PD)模型。因此,临床试验的架构正在经历深刻变革,以确保患者安全和科学严谨。
生物标志物驱动的给药与PK/PD模型
在传统的体外临床试验中,研究人员施用精确计量的活体工程CAR-T细胞。相比之下,体内CAR-T临床试验施用的是载体颗粒剂量(如病毒基因组或LNP质量)。随后的体内转导效率和新生成的CAR-T细胞的扩增峰值在很大程度上取决于患者独特的免疫基线。因此,现代临床试验必须纳入复杂的液体活检监测,利用高分辨率多参数流式细胞术和下一代测序,动态追踪载体生物分布、T细胞转导率和实时CAR蛋白表达。
安全性控制:靶向非肿瘤毒性与免疫原性
基因递送载体的全身给药引入了独特的安全性考虑,必须在临床试验期间进行细致管理。
- 靶向非肿瘤毒性(On-Target Off-Tumor Toxicity): 如果递送载体错误地转导了非靶标细胞(如巨噬细胞或调节性T细胞),可能导致严重的脱靶毒性或悖论性免疫抑制。在早期临床试验中,严格的生物标志物筛选和组织活检对于验证载体嗜性至关重要。
- 载体免疫原性: 患者可能带有针对病毒衣壳或LNP脂质成分的预存中和抗体。此外,mRNA平台通常需要的重复给药可能触发抗药物抗体(ADA)。管理这一问题需要在临床试验方案中整合精准的免疫调节方案。
- 安全开关: 为了降低不受控的体内增殖和危及生命的CRS风险,下一代构建体通常包含小分子门控的“安全开关”。这些工程逻辑门允许临床试验研究人员在出现严重毒性时迅速停止CAR-T活性或诱导细胞凋亡。
15年长期随访(LTFU)要求
由于整合型载体(如慢病毒)具有插入突变的内在风险以及引发继发性原发肿瘤(SPM)的理论可能,全球监管机构严格要求进行详尽的长期监测。体内CAR-T临床试验的申办方必须建立强大的数据登记基础设施,能够在输注后追踪患者长达15年。这需要无缝整合临床数据管理系统,以在主要临床试验终点达成后长期维持数据完整性。
演进中的全球监管框架:2026年美国FDA CMC灵活性
为支持复杂细胞和基因药物的爆发式增长,监管机构正在调整其监督机制。2026年1月11日,美国FDA生物制品评价与研究中心(CBER)发布了开创性指南,在细胞和基因疗法的化学、制造和控制(CMC)要求方面提供了前所未有的监管灵活性。
FDA局长Marty Makary博士表示,这些常识性改革旨在拆除行政障碍并促进快速创新。根据这一新框架,进行II期和III期临床试验的申办方不再被要求严格遵守21 CFR part 211中繁琐的商业制造标准。此外,如果申办方在临床试验后期对制造工艺进行微调,FDA现在将接受精简的可比性数据,而非要求进行大规模、耗时的重新验证研究。这一范式转变大幅减少了体内CAR-T资产从首次人体临床试验到商业上市所需的时间和资金。
| 监管领域 | 传统FDA CMC预期 | 2026年FDA对CGT临床试验的CMC灵活性 |
| II/III期制造 | 完全符合商业21 CFR part 211标准 | 根据21 CFR 210.2(c)获得广泛豁免 |
| 产品放行标准 | 早期即需严格、确定的规格 | 临床试验期间允许宽松的接受标准 |
| 工艺变更 | 繁重且受限的可比性数据要求 | 通过精简的可比性数据快速批准细微变更 |
| 验证要求 | 强制提交三(3)批PPQ批次 | 免除三批PPQ要求,拥抱生命周期演进 |
《生物安全法案》与临床试验供应链的地缘政治重组
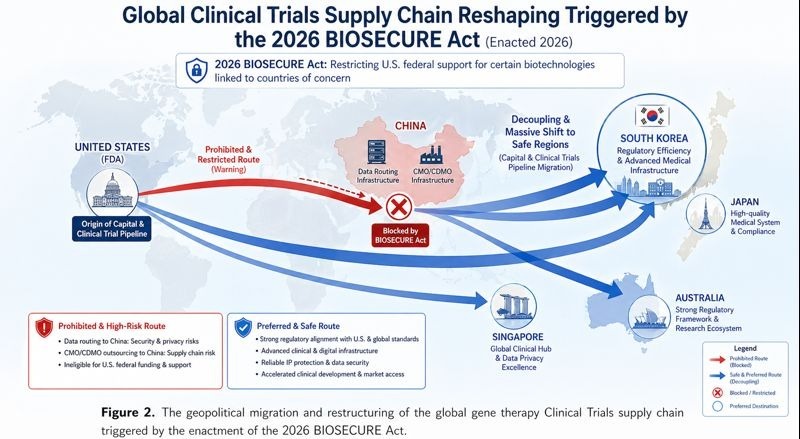
在技术和监管进步推动行业发展的同时,一场巨大的地缘政治动荡正同步重塑全球临床试验格局。于2026年正式生效并全面执行的美国《生物安全法案》(BIOSECURE Act),禁止接受联邦资助的机构使用由指定的、与外国对手有关联的“受关注生物技术公司”提供的生物技术设备、服务或数据平台。
国会调查揭示了对某些外国军事关联医疗机构的担忧,指称其挪用了西方制药临床试验的多组学和基因组数据。由于体内CAR-T临床试验严重依赖密集的基因组测序、患者免疫分型和高分辨率生物标志物追踪,全球申办方正在积极终止与相关CDMO和临床研究组织(CRO)的合同。这一立法指令引发了全球临床试验供应链的紧急、大规模脱钩,迫使申办方迅速将其高度敏感的基因药物组合转移到安全的、美国盟友的临床中心。
亚太中心:韩国临床试验竞争力与全球CRO策略
随着《生物安全法案》迫使先进研发进行快速地理重组,韩国已牢固确立其作为下一代临床试验首选替代目的地的地位。凭借卓越的监管环境、高度集中的医疗基础设施和无可挑剔的数据完整性标准,韩国始终稳居全球临床试验前四大中心之列。
无与伦比的监管效率与启动时间
在验证体内CAR-T疗法的激烈竞赛中,上市时间是核心竞争力。韩国食品医药品安全部(MFDS)运行着高效的监管机制,允许IND行政审查与医院级机构审查委员会(IRB)伦理审查并行开展。这种简化流程使得从获得批准到首例患者入组(FPI)的平均启动时间仅为6至8周。
顶尖基础设施与高患者密度
首尔凭借密集的顶级三级学术医院网络,依然是无可争议的全球临床试验活动中心。像首尔大学医院(SNUH)这样的机构在短短五年内执行了超过945项早期癌症临床试验。这些巨型医院配备了专有的AI驱动临床决策支持系统(如KMed.AI)和完全适合转化研究的内部GMP设施。对于需要24/7 ICU支持和快速干预协议以管理潜在神经毒性或CRS的复杂体内CAR-T临床试验,韩国的临床基础设施提供了无与伦比的安全性和运营执行力。
通过全球CRO实现的综合临床试验操作系统
在这一复杂的格局中航行需要该地区专业全球合同研究组织(CRO)的专长。现代CRO充当临床试验的综合“操作系统”,无缝协调跨境物流、应对地方MFDS法规并确保严格遵守ICH GCP。韩国的临床数据被FDA和EMA广泛接受用于关键的全球申报,确保申办方最大化其开发项目的投资回报率(ROI)。
| 关键绩效指标 | 韩国临床试验指标 | 全球申办方的战略优势 |
| 试验启动时间线 | 6至8周(IND/IRB并行审查) | 比亚太其他地区快数月;加速上市 |
| 全球排名 | 整体试验活跃度全球前4 | 拥有快速、可靠患者招募能力的成熟生态系统 |
| 基础设施密度 | 超过220家MFDS认证的巨型医院 | 高效执行复杂的、多中心方案 |
| 数据完整性与认可度 | 完全符合ICH GCP标准 | 数据获FDA和EMA无条件接受,用于BLA申请 |
结论:完成基因药物革命
体内CAR-T技术的出现代表了细胞免疫治疗的最后前沿,系统性地拆除了长期困扰体外制造的物流、财务和生物学障碍。礼来公司在2026年初以总计94亿美元收购Kelonia Therapeutics和Orna Therapeutics,明确释放出制药行业正积极转向针对癌症和自身免疫性疾病的原位细胞重编程的信号。
然而,成功将这些颠覆性模式商业化需要应对临床试验中一系列全新的挑战。从建立复杂的生物标志物驱动给药协议到管理15年的纵向安全性登记,临床申办方的运营需求从未如此之高。在FDA新的CMC灵活性指南和《生物安全法案》强制要求的地缘政治脱钩背景下,执行全球临床试验需要无与伦比的战略前瞻性。对于有远见的生物制药申办方而言,利用韩国卓越的速度、临床基础设施和不妥协的数据完整性已不再仅仅是一个选项,而是引领全球基因药物革命的必然选择。
您准备好优化您的体内CAR-T临床试验设计了吗? 开发下一代细胞和基因疗法需要应对复杂的生物标志物策略、严格的长期随访协议以及迅速变化的全球法规。与我们在韩国的世界级CRO专家合作,体验无与伦比的执行速度——仅需6至8周即可启动试验。立即通过符合FDA标准的数据完整性最大化您的临床ROI。
紧跟全球临床试验情报前沿! 不要错过关于FDA CMC监管灵活性、大药企并购动态以及亚太临床格局独家见解的最新更新。订阅我们的高级见解,直接在收件箱中接收专家分析。
常见问题解答 (FAQs)
Q1. 体内CAR-T临床试验与传统的体外CAR-T研究有何根本区别? A1. 在传统的体外临床试验中,患者的T细胞必须被提取、运输到实验室、进行基因改造、扩增然后再回输,这个昂贵的过程需要数周。体内CAR-T临床试验完全绕过了这一过程,通过直接向患者血液注入专门的基因递送载体(如LNP或慢病毒),现场对免疫细胞进行编程。这消除了复杂的制造物流和严苛的预处理化疗,大大缩短了治疗时间。
Q2. 礼来公司同时收购Kelonia和Orna Therapeutics对其未来临床试验有何战略意义? A2. 礼来战略性地收购这两家公司是为了在其未来的临床试验中主导两个不同的治疗领域。Kelonia(以高达70亿美元收购)利用慢病毒载体将CAR基因永久整合到T细胞中,这对于多发性骨髓瘤等持久性癌症疗法非常有效。相反,Orna Therapeutics(24亿美元)使用LNP内的环状RNA来驱动瞬时CAR表达,使其在自身免疫性疾病临床试验的免疫重置策略中表现出卓越的安全性和有效性。
Q3. 在体内CAR-T临床试验中监控的最关键安全性参数是什么? A3. 由于基因编辑载体是全身给药,开展临床试验的研究人员必须严格监控“靶向非肿瘤”毒性以及载体在肝脏等器官中的意外蓄积。此外,管理递送载体的免疫原性(如抗药物抗体)并降低病毒载体带来的插入突变风险,需要整合安全开关和强制性的15年长期随访(LTFU)观察协议。
Q4. 2026年FDA CMC指南如何影响先进基因疗法临床试验的时间线? A4. FDA 2026年1月的指南引入了显著的监管灵活性以加速创新。对于进行II期和III期临床试验的申办方,FDA放宽了对商业21 CFR part 211制造标准的严格遵守要求。此外,临床试验后期的细微制造变更现在可以通过精简的可比性数据获得批准,从而大幅减少达到商业化所需的时间和资金负担。
Q5. 为什么在《生物安全法案》之后,韩国正成为全球临床试验的首选中心? A5. 美国《生物安全法案》出于数据安全考虑,严厉限制了与特定外国实体的合作,迫使申办方将其高度敏感的基因临床试验移出相关地区。韩国成为首选替代方案,是因为它提供高度先进的医疗基础设施、不妥协的ICH GCP数据完整性(获FDA完全认可),以及极具效率的并行监管审查流程,使申办方能在短短6至8周内启动临床试验。