为什么“Pan-RAS 抑制剂载荷 ADC”突然成为热议焦点
在过去 1-2 个月中,肿瘤研发对话中出现频率最高的一个词不再是“又一款 ADC”,而是载荷(Payload)本身的变革。自 2026 年 AACR(美国癌症研究协会)年会以来,行业的重心已进一步从“我们要瞄准哪个抗原?”转向“我们要递送什么机制、如何递送以及这种递送的可控性如何?”
在这种背景下,Pan-RAS 抑制剂载荷具有高度的象征意义。RAS 一直是肿瘤生物学和药物研发的支柱,但也极其难攻——尤其是涉及广泛的通路抑制时。抑制概念越广泛,耐受性和安全性窗口就越敏感。这就是为什么最近的讨论已超越“开发一种新抑制剂”,转向“我们能否重新设计抑制机制的操作方式,从而重建治疗窗口?”。其中一种方法是将机制型小分子转化为 ADC 载荷,以便更具选择性地递送至肿瘤细胞。
从“靶点竞争”转向“载荷竞争”
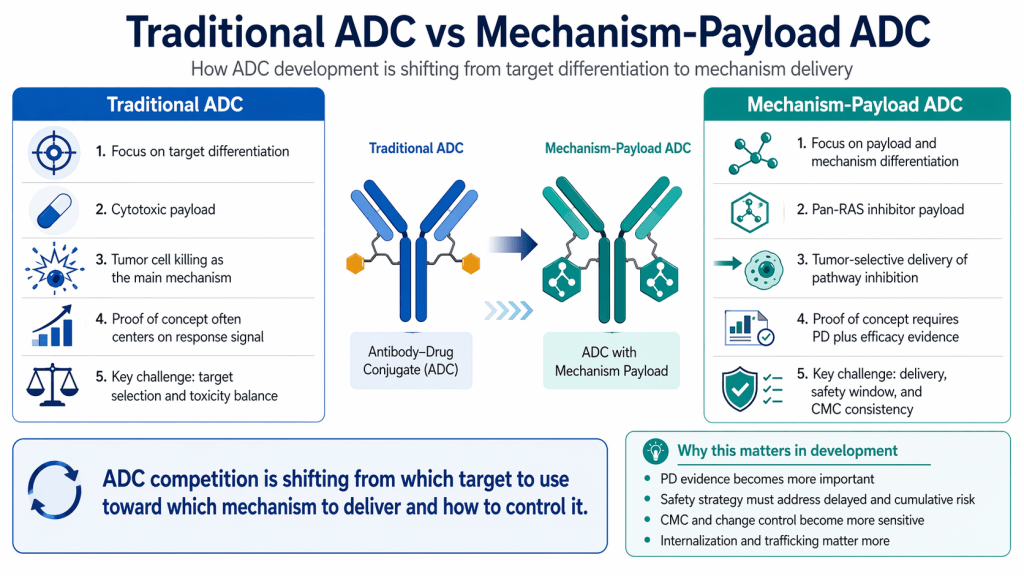
传统 ADC 的逻辑很直接:连接强效细胞毒性载荷,结合肿瘤细胞,内吞,释放载荷,杀死细胞。当临床缓解出现时,故事往往极具说服力且直观。
而通路机制载荷(如 Pan-RAS 抑制剂)改变了这一逻辑。对于通路抑制,成功通常取决于暴露时间、组织分布、代谢以及对正常组织的影响。将这种机制转化为载荷不仅仅是“装载毒性”,而是尝试通过递送设计来重新调整该机制运作的地点和强度。
这也解释了为什么这种方法不能仅仅依赖结合。它需要一致的内吞、可预测的细胞内处理和可靠的释放行为——因为这些步骤决定了载荷是否能在正确的细胞中达到有效的细胞内暴露。这就是为什么双旁位(Biparatopic)结合等设计经常出现在同一叙事中。简而言之:随着载荷变得更加复杂,抗体平台的递送性能变得更加核心。
为什么机制载荷 ADC 在实际开发中更难
将其视为一个“理应有效的酷概念”很诱人,但开发过程很少会自动变得容易。相反,它催生了新的实际问题——这些问题在论文中并不耀眼,但往往决定了一个项目是进展顺利还是陷入停滞。
在机制载荷 ADC 中,临床设计、安全性策略、CMC 决策和数据运营并非独立运行。机制可能使疗效和安全性在同一轴线上移动,制造或可比性变更可能演变为解释风险,而数据对齐问题会直接削弱证据的可信度。这里的“复杂性”并非抽象词汇,它意味着构建和辩护证据叙事的难度增加了。
申办方应规划的四个开发转变
1. 概念验证不能仅靠 ORR:PD 成为骨干
对于细胞毒性载荷 ADC,早期 PoC(概念验证)有时可以严重依赖可见的缓解信号。但在 Pan-RAS 抑制剂载荷中,问题会来得更快:“这真的是 RAS 通路抑制吗?”“抑制是否持久?”“谁获益最大,为什么?”这些问题在全球评审和授权交易讨论中更为核心。
实际上,PD(药效学)不应被视为可有可无的附件。对于机制载荷 ADC,PD 应成为项目解释结构的一部分。这意味着要定义测量什么、何时测量(不仅仅仅是一个时间点),以及如何将 PD 变化与临床结果联系起来(包括响应者与非响应者的模式)。当这一骨干强大时,有限的缓解信号仍具备可解释性,而强大的缓解则更具防御性,被视为可重复的生物学结果而非运气。
2. 安全性并非“自动提升”:可能出现新的毒性模式
“肿瘤选择性递送”是一个强大的承诺,但并非保证。安全性仍可能受到正常组织靶点表达、载荷释放与代谢以及实际旁观者效应程度的影响。
因此,安全性策略不应止于“典型的 ADC 毒性”。应假设延迟和累计风险可能至关重要,并据此设计监测。实际目标不是“监测更多”,而是“更聪明地监测”:定义哪些信号重要、审阅频率以及适用哪些升级规则。如果早期定义了这些规则,安全性数据将累计成结构化的叙事,而非一堆混乱的事件。
3. CMC 和变更控制不容推迟:载荷变更可能导致项目变更
机制型载荷的行为更像“药物本身”。接头、载荷或工艺的微小变化都可能引发关于疗效和安全性影响的更强烈质疑。许多团队试图通过推迟 CMC 严谨性来换取速度,但这类药物可能会在后期对这种做法进行惩罚。
实际的转变在于,批次一致性、放行规格的依据以及不可避免变更的桥接逻辑应更早地思考清楚。这不仅是为了监管机构,对商务发展(BD)也至关重要,因为合作伙伴正在评估该平台是否可以扩展到多个资产。CMC 和变更控制不仅仅仅是“工厂问题”,它们可能演变为交易价值和开发风险问题。
4. 內吞与运输的变异性影响更深远
对于这些项目,细胞内递送和处理的程度及一致性可直接决定结果。仅有高靶点表达可能不足够。细胞处理能力的差异、肿瘤微环境以及现实生物学与临床前递送假设的匹配程度都至关重要。
因此,临床策略可能日益围绕一个更尖锐的问题:在哪些患者群体中,递送的可靠性足以使机制得到一致证实?如果这个问题回答得好,PoC 概率就会提高,数据也会更干净。否则,项目可能在不同中心或亚组之间显得不稳定,解释成本随之上升。
中国开发者规划海外试验的实际洞察
对于中国团队来说,机制载荷 ADC 极具吸引力:差异化明确,授权故事更容易讲。但它们也可能被归类为高风险资产,这意味着海外合作伙伴和投资者往往要求有一套解释和控制风险的系统。海外试验不应被视为“在另一个国家做同样的研究”,而应被视为构建一套全球通用的证据包。
在实践中,如果预先设计好以下六个要素,海外 PoC 将变得顺畅得多: 第一,PD/机制证据计划(样本、时间、检测方法)。 第二,围绕延迟和累计风险假设建立的安全性监测结构。 第三,CMC 一致性和带有桥接逻辑的基本变更控制原则。 第四,中心实验室准备就绪及样本可追溯性。 第五,EDC–Safety–PK/PD 的对账节奏,确保证据保持连贯。 第六,多标准的 Go/No-go 阈值(不限于 ORR)。
这些并非为了产生更多文件,而是为了建立一个在项目扩展时保持稳定的操作系统——从而使下一个项目运行得更快,并降低回答合作伙伴问题的成本。
结论:2026 年,载荷机制正在成为关键的开发语言
以 Pan-RAS 抑制剂载荷概念为代表的机制载荷 ADC 表明,ADC 正在从细胞毒性载体向机制递送平台扩展。这一转变改变了 PoC 证据的形式、安全性叙事、CMC 和变更控制预期,以及保持故事连贯所需的数据治理。随着时间的推移,核心问题将不再是“靶点是什么?”,而更多是“你递送的是什么机制,以及你如何证明并控制它?”
Intoinworld 是一家总部位于韩国的 CRO,在 I-IV 期临床和上市后研究方面拥有超过 10 年的本地执行经验。如果您正在规划海外 PoC 或为创新疗法(包括 ADC)进行全球化执行准备,我们可以提供端到端的支持,包括 IND/IRB 准备、中心运营、数据管理和安全性运营。请使用本页面的“报价”按钮索取报价。



