近年来,韩国已经逐渐从亚洲区域性临床试验市场,发展成为全球创新药研发的重要战略中心。特别是在肿瘤、抗体偶联药物、细胞与基因治疗、免疫治疗以及罕见疾病领域,越来越多国际制药公司与生物科技企业开始将韩国纳入核心临床开发计划之中。
对于许多海外申办方而言,韩国的吸引力十分明显。大型综合医院体系、高度数字化医疗环境、丰富的患者资源、经验成熟的研究团队以及相对高效的监管环境,都让韩国成为越来越重要的全球临床试验目的地。
但真正进入韩国市场之后,许多全球企业很快便会发现,韩国临床试验真正复杂的部分,很多时候并不是监管审批,而是韩国医院内部如何实际处理全球临床试验。
很多海外企业在欧美市场已经积累了丰富经验,因此往往会习惯性地认为韩国医院的运营逻辑与欧美市场相似。然而,韩国大型医院拥有自己独特且高度复杂的运营体系,而这种内部运营模式,往往才是真正影响临床试验启动速度、医院启动效率以及患者招募时间的关键。
为什么韩国医院越来越受到全球申办方重视?
韩国近年之所以快速成为全球临床试验重要市场,并不仅仅因为监管效率提升,更重要的是韩国医院本身已经建立了非常成熟的国际研究体系。
尤其首尔大型综合医院,通常同时具备先进医疗基础设施、集中患者资源以及丰富国际研究经验。很多大型医院长期参与全球多中心研究,因此无论研究者、研究协调员还是临床试验中心,对于国际项目流程都已经相当熟悉。
与此同时,韩国在肿瘤、抗体偶联药物以及细胞与基因治疗领域的发展速度也非常快。越来越多全球创新药项目选择优先进入韩国开展临床试验,原因之一便是韩国医院在复杂研究领域已经累积大量执行经验。
韩国政府与韩国食品药品安全处近年来也持续推动全球创新药与国际研究支持政策,包括加速审查机制、数字医疗建设以及国际研发投资支持等,这些都进一步提升了韩国作为全球临床试验市场的竞争力。
因此,现在对于很多国际申办方而言,韩国已经不再只是亚洲市场,而是全球临床开发战略中的核心国家之一。
韩国医院实际上如何运营国际临床试验?
很多海外企业第一次进入韩国时,都会低估韩国医院内部运营结构的复杂度。
在欧美部分市场中,研究者往往拥有较高自主权,但韩国大型医院通常属于高度集中化管理体系。一个国际临床试验进入医院之后,并不是单纯由研究者决定即可启动,而是需要多个部门同时参与协调。
通常情况下,一个全球临床试验项目会同时涉及:
临床试验中心、伦理委员会、法务部门、财务部门、药房、研究协调员、检验部门以及医院行政团队。
这意味着,即使研究者本身已经愿意参与项目,研究仍然可能因为医院内部流程尚未完成而无法正式启动。
例如:
合同尚未完成审核、预算尚未批准、药房流程未确认、文件格式不符合医院要求、伦理委员会需要补件等情况,都可能导致项目延迟。
很多海外企业过去会认为韩国临床试验的关键在于监管审批,但真正进入执行阶段后才会发现,韩国医院内部运营流程才是最容易影响整体时间线的部分。
韩国临床试验真正的启动流程是什么?
许多海外申办方会把韩国临床试验理解为:
获得韩国食品药品安全处批准之后,医院即可开始患者招募。但实际上,韩国真实的临床试验启动流程远比想象复杂。
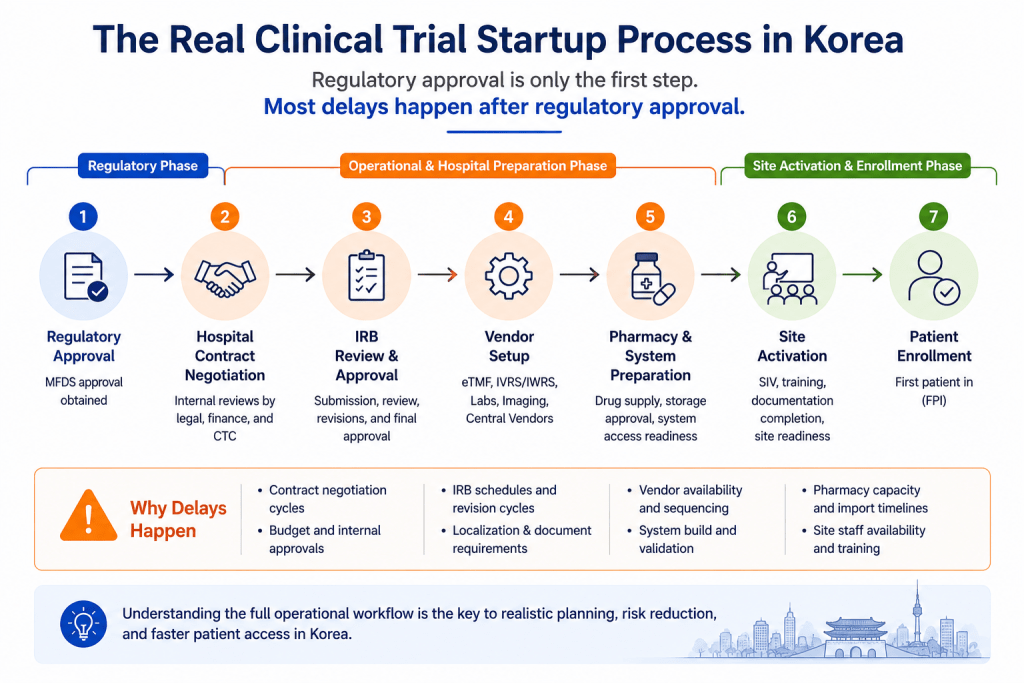
通常情况下,项目即使已经完成监管审批,后续仍然需要经历医院合同谈判、伦理委员会提交、供应商设置、药房准备、研究人员安排以及内部行政确认等多个阶段。
真正的患者入组,往往发生在所有运营准备完成之后。
因此,韩国临床试验中一个非常重要的现实是:
监管批准并不等于项目已经具备实际启动条件。
很多全球项目虽然已经获得批准,但由于合同尚未完成、供应商时间线不同步、电子系统尚未建立或医院内部准备尚未结束,最终仍然无法快速启动。
对于全球申办方而言,真正影响项目速度的,很多时候不是审批,而是审批之后的大量运营协调工作。
为什么韩国医院合同谈判经常需要更长时间?
很多海外企业进入韩国市场后,最意外的问题之一,就是医院合同流程通常比预期更长。
许多国际申办方过去会认为合同只是简单法务审核,但韩国大型医院的合同流程通常涉及多个部门,包括临床试验中心、法务部门、财务部门以及预算审核部门等。
更重要的是,这些部门很多时候并不会同步工作,而是依照医院内部流程逐步推进。
特别是在肿瘤、抗体偶联药物以及细胞与基因治疗研究中,由于项目复杂度较高、预算项目较多,因此合同讨论往往需要更长时间。
近年来,随着全球研究数量快速增加,韩国大型医院对于研究资源与人员安排也变得更加谨慎,因此合同谈判时间普遍比过去更长。
在很多国际项目中,真正拖慢整体启动速度的,并不是监管审批,而是医院合同与内部协调流程。
韩国伦理委员会为什么经常成为关键时间因素?
韩国大型医院伦理委员会通常拥有固定提交周期与严格文件要求。
不同医院之间,无论是提交时间、审查频率、文件格式还是患者文件表达方式,都可能存在明显差异。
如果项目错过提交窗口,整体时间线便可能直接延迟数周。
与此同时,韩国医院对于患者相关文件的本地化质量要求非常高。
很多海外企业会认为,只要将英文文件翻译成韩文即可提交,但实际上,韩国医院更重视:
医疗术语是否符合韩国临床环境、患者是否容易理解、文件表达是否自然以及格式是否符合医院规范。
因此,即使只是细微文字差异,也可能导致伦理委员会要求重新修改文件。
很多国际研究项目的启动延迟,实际上并不是因为监管问题,而是因为本地化问题。
韩国大型医院为什么不一定代表更快?
很多海外企业会认为,只要选择韩国顶级医院,患者招募速度便一定会很快。 但现实情况是,大型医院同时也在参与大量国际研究。
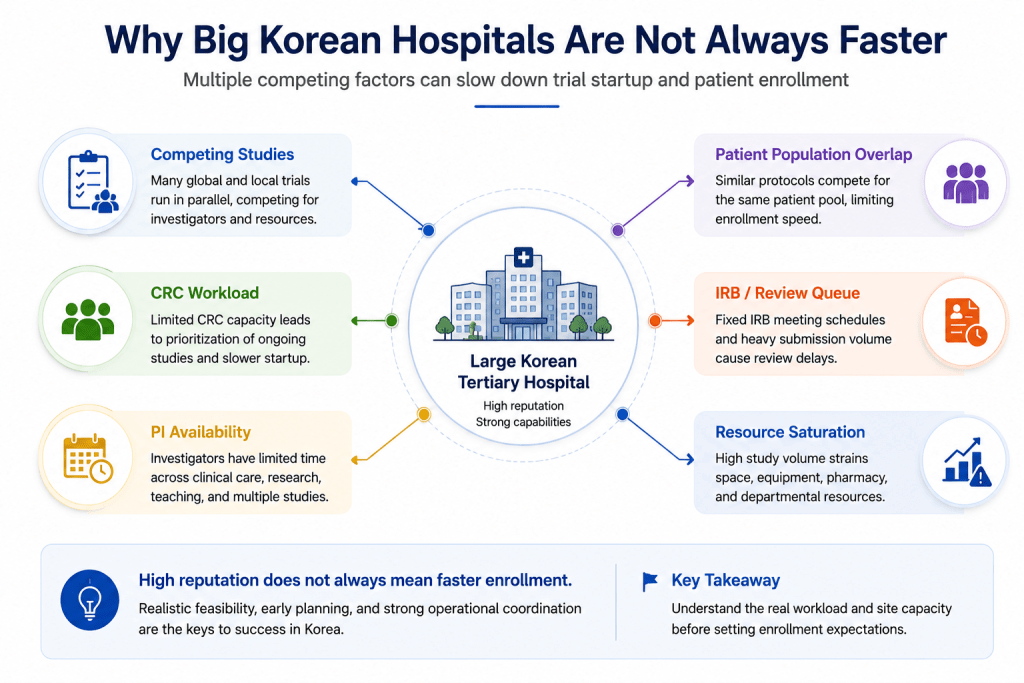
特别是在肿瘤领域,同一家医院往往同时运行多个全球第三期研究、免疫治疗项目以及抗体偶联药物研究。
因此,即使医院本身研究能力非常强,也可能因为研究协调员工作负荷过高、研究者时间有限、患者池重叠以及竞争性研究增加等原因,而导致患者招募速度低于预期。
所以,真正重要的并不是医院名气本身,而是:
当前研究负荷、竞争研究情况、患者实际可及性以及项目可行性评估是否现实。
很多项目后续出现延迟,并不是因为医院不好,而是因为前期可行性评估过于理想化。
为什么韩国临床试验越来越重视运营协调能力?
过去很多国际申办方会认为,临床试验服务公司的主要工作只是监管申报。
但实际上,在韩国市场,真正重要的能力往往是运营协调。
特别是在国际多中心研究中,一个项目通常同时涉及多个供应商、多个医院以及不同系统平台。
只要其中一个环节出现问题,整个启动流程便可能受到影响。
例如:
合同延迟可能导致伦理委员会提交延迟,而伦理委员会延迟又可能进一步影响供应商设置、医院启动以及患者招募时间。
这种高度互相依赖的运营结构,正是韩国临床试验的重要特点之一。
因此,现在越来越多全球申办方开始意识到:
韩国临床试验成功的关键,已经不仅仅是监管审批速度,而是整体运营执行能力。
真正理解韩国医院如何运营国际临床试验的团队,通常更能够减少启动延迟、提高医院合作效率并降低整体运营风险。
结论:理解韩国医院运营方式,比单纯理解法规更重要
韩国仍然是全球最具战略价值的临床试验市场之一。特别是在肿瘤、抗体偶联药物、细胞与基因治疗以及早期临床研究领域,韩国大型医院体系、研究经验以及数据质量依然拥有非常强的国际竞争力。
但与此同时,随着国际研究数量持续增加,韩国医院内部运营复杂度与资源竞争也正在不断上升。
对于全球申办方而言,未来真正重要的已经不仅仅是如何获得韩国监管批准,而是如何真正理解韩国医院如何运营全球临床试验。
因为在韩国市场,真正决定项目执行效率的,很多时候并不是监管本身,而是运营协调能力。
正在规划韩国临床试验?
随着韩国在肿瘤、抗体偶联药物、细胞与基因治疗以及全球创新药开发中的战略地位不断提升,越来越多国际申办方正在重新评估韩国临床试验布局。
如果您正在评估韩国临床试验可行性,或希望更深入了解韩国医院真实运营模式、韩国临床试验启动流程、医院选择策略以及肿瘤与抗体偶联药物研究执行环境,欢迎与 Intoinworld 团队交流。
我们可协助全球申办方评估韩国临床试验启动策略、运营可行性与本地执行方向。
👉 联系我们,讨论您的韩国临床试验策略。

