2026년 pan-RAS 억제제 페이로드 ADC 트렌드: AACR 2026이 보여준 임상·안전성·CMC 핵심 포인트
최근에 왜 ‘pan-RAS 억제제 페이로드 ADC’가 갑자기 많이 언급되나
최근 oncology R&D에서 눈에 띄게 늘어난 표현이 있습니다. “ADC가 또 나온다”가 아니라, 페이로드 자체가 바뀌고 있다는 이야기입니다. 특히 AACR 2026 이후로는 “표적”보다 “payload가 어떤 기전을 싣는지”가 개발 전략의 중심으로 올라오는 분위기가 더 강해졌습니다. 예전에는 어떤 항원을 선택하느냐가 차별화의 1순위였다면, 이제는 같은 표적을 보더라도 “무슨 페이로드를, 어떤 방식으로, 어느 정도 통제 가능하게 싣느냐”가 경쟁력의 핵심 언어로 바뀌고 있습니다.
여기서 pan-RAS 억제제 페이로드는 상징성이 큽니다. RAS 계열은 항암 개발에서 ‘항상 중요하지만 동시에 항상 어려운’ 축으로 남아 있었고, 특히 pan-RAS는 범위를 넓히는 만큼 안전성·내약성의 부담이 더 커질 수 있는 영역입니다. 그래서 최근에 나오는 논의는 단순히 “새 억제제를 만들자”가 아니라, 억제제의 전달 방식 자체를 바꿔서 치료 창을 다시 설계해 보자로 흘러가고 있습니다. 그 시도 중 하나가 “기전형 소분자 억제제를 ADC payload로 만들어 종양에 더 선택적으로 전달한다”는 컨셉입니다.
“타깃 경쟁”에서 Payload 경쟁으로
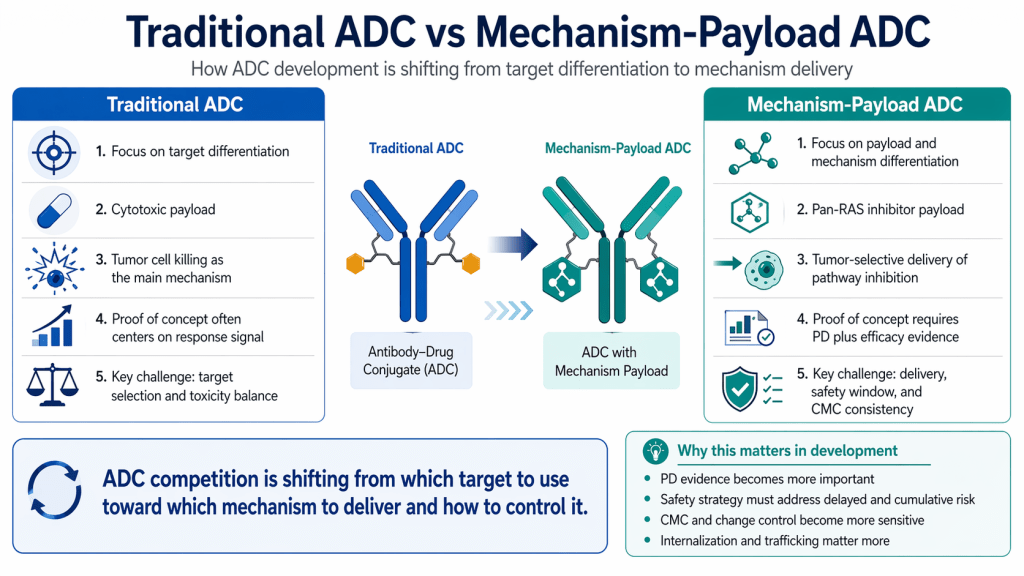
전통적인 ADC는 강한 세포독성 페이로드를 싣고 종양세포에 들어가 터뜨리는 방식이 많았습니다. 그래서 임상에서 반응이 나오면 비교적 직관적으로 설득할 수 있었습니다. 반면, pan-RAS 억제제처럼 “신호전달을 조절하는 기전”은 원래 약물의 노출 시간, 분포, 대사, 정상조직 영향 같은 요소에 의해 성패가 갈리기 쉽습니다. 이 기전을 페이로드로 바꾼다는 것은, 단순히 “독성을 싣는다”가 아니라 기전의 작동 위치와 작동 강도를 ‘전달 설계’로 재조정한다는 의미가 됩니다.
이 접근이 성공하려면, “표적에 잘 붙는다”만으로 부족합니다. 종양세포 내부로 얼마나 잘 들어가고, 얼마나 일정하게 가공되고, 그 결과 페이로드가 얼마나 예측 가능하게 방출되는지가 성능을 좌우합니다. 그래서 최근 자료에서 biparatopic 같은 설계가 같이 언급되는 경우가 많습니다. 쉽게 말해, ‘페이로드가 복잡해질수록 운반체(항체)의 전달 성능이 더 중요해진다’는 논리입니다.
‘기전형 페이로드 ADC’가 임상에서 어려워지는 이유
Pan-RAS 억제제 페이로드 ADC가 흥미롭다고 해서, 임상이 자동으로 쉬워지지는 않습니다. 오히려 개발팀이 새로 풀어야 할 질문이 늘어납니다. 그 질문들은 대개 “논문에서 멋있게 보이는 질문”이 아니라, 실제로 프로그램이 중간에 멈추는 원인이 되는 실무 질문입니다. 그래서 이 트렌드를 읽을 때는 “왜 뜨는가” 다음으로 “어디서 깨지는가”를 함께 봐야 합니다.
임상 설계, 안전성, CMC, 데이터 운영이 서로 분리되지 않습니다. 기전형 페이로드는 ‘효능’과 ‘안전성’이 같은 축에서 흔들리기 쉽고, CMC 변경이나 데이터 정합성 문제도 곧바로 해석 리스크로 연결될 수 있습니다. 즉, 개발이 ‘복잡해진다’는 말은 추상적인 표현이 아니라, 증거를 만들고 설명하는 작업의 난도가 올라간다는 뜻입니다.
임상개발 관점에서 달라지는 4가지 핵심 포인트
1) PoC는 ORR 하나로 끝나기 어렵다: PD(기전 증거)가 ‘척추’가 된다
세포독성 페이로드 중심 ADC는 임상 초기에 “반응이 나왔다”는 사실 자체가 강한 설득력이 될 때가 많습니다. 하지만 pan-RAS 억제제 페이로드는 조금 다릅니다. 단순히 종양 크기가 줄었다고 해도, “그게 정말 RAS 경로 억제 때문인지”, “얼마나 지속적으로 억제됐는지”, “어떤 환자에서 더 잘 작동하는지”를 묻는 질문이 훨씬 빨리 따라옵니다. 특히 해외 파트너나 글로벌 심사 관점에서는 이 질문이 더 강하게 들어옵니다.
그래서 이 계열에서는 PoC를 설계할 때부터 PD를 ‘추가 자료’로 붙이는 게 아니라, 프로그램의 설명 구조 자체로 넣는 편이 좋습니다. 예를 들어, 어떤 샘플을 언제 채취할지(투여 직후, 일정 시간 후, 반복 시점), 어떤 지표로 경로 억제를 확인할지, 그 지표가 임상 반응과 어떻게 연결될지(반응자/비반응자 비교) 같은 것들이 초기에 정리돼야 합니다. 이 작업이 잘 되어 있으면, 반응이 다소 제한적이더라도 “왜 그런지”를 설명할 수 있고, 반응이 좋을 때는 “재현 가능성”을 더 설득력 있게 주장할 수 있습니다.
2) 안전성은 ‘자동으로 좋아질 것’이라 가정하면 위험하다: 새로운 독성 패턴이 나올 수 있다
기전형 페이로드 ADC는 ‘종양 선택적 전달’이라는 강력한 서사를 갖습니다. 하지만 임상에서는 그 서사가 그대로 안전성 개선으로 이어진다고 단정하기 어렵습니다. 이유는 단순합니다. 표적이 정상조직에 어느 정도 존재할 수 있고, 페이로드의 방출/대사 과정에서 시스템 노출이 생길 수 있으며, bystander effect가 어디까지 영향을 미치는지에 따라 실제 독성 양상이 달라질 수 있기 때문입니다.
그래서 안전성 전략은 “ADC니까 이런 독성” 정도로 끝내면 안 됩니다. 오히려 pan-RAS라는 기전 특성을 고려해, 지연 독성과 누적 독성 가능성을 초기에 가정하고 설계하는 편이 더 안전합니다. 모니터링 항목도 단순 AE 리스트가 아니라, 기전과 연관된 잠재 리스크를 중심으로 구조화해야 합니다. 여기서 실무적으로 중요한 건 “많이 모니터링”이 아니라 “어떤 신호를 어떤 주기로, 어떤 기준으로 escalations 할지”를 미리 정해두는 것입니다. 그래야 데이터가 쌓일수록 안전성 서사가 ‘정리된 형태’로 남습니다.
3) CMC와 변경관리는 뒤로 미루면 늦다: payload 변경 = 프로그램 변경이 될 수 있다
기전형 페이로드는 말 그대로 ‘약의 본체’ 성격이 더 강합니다. 그래서 linker/payload/공정이 조금만 바뀌어도, 그 변화가 효능·안전성에 미치는 영향에 대한 질문이 더 빨리, 더 강하게 들어올 가능성이 높습니다. 많은 팀이 초기에는 속도를 위해 CMC를 ‘나중에 정교화’하려고 하지만, 이 유형에서는 그런 접근이 리스크가 될 수 있습니다.
실무적으로는 다음이 중요해집니다. 배치 간 일관성을 어떤 지표로 관리할지, release spec을 어떻게 합리화할지, 그리고 변경이 발생했을 때 어떤 논리로 브릿징을 할지(혹은 어떤 변경은 피해야 하는지)를 비교적 초기에 정리해야 합니다. 이건 규제 대응을 위해서만이 아니라, BD에서도 매우 중요한데, 파트너는 결국 “이 플랫폼을 여러 자산으로 확장할 수 있나”를 보고 싶어하기 때문입니다. 즉, CMC/변경관리는 ‘공장 문제’가 아니라 딜 밸류와 연결되는 개발 리스크입니다.
4) ‘내재화/trafficking’ 변수가 더 커진다: 환자 선택 논리도 더 정교해진다
이 유형은 세포 안으로 얼마나 잘 들어가고, 세포 안에서 어떤 경로로 처리되며, payload가 얼마나 예측 가능하게 방출되는지가 성능을 좌우할 수 있습니다. 즉, 단순히 “표적 발현이 높다”가 충분하지 않을 수 있습니다. 같은 발현이라도 세포의 처리 능력, 종양 미세환경, 전임상에서 기대했던 전달 경로가 임상에서 동일하게 재현되는지 등이 영향을 줄 수 있습니다.
그래서 임상 전략은 자연스럽게 “어떤 환자군에서 전달이 안정적으로 일어나는가”를 더 세밀하게 묻는 쪽으로 이동할 수 있습니다. 이 부분을 잘 풀면 장점이 있습니다. 환자 선택이 더 정교해질수록 PoC의 성공 확률이 올라갈 수 있고, 데이터가 깔끔해질 수 있습니다. 반대로 여기서 헤매면, 같은 약이라도 센터/환자군에 따라 결과가 흔들리는 것처럼 보일 수 있어 해석 비용이 커집니다.
해외 임상을 고민하는 중국 개발사에게 주는 인사이트
중국 개발사 입장에서 기전형 페이로드 ADC는 매우 매력적인 자산입니다. 차별화 포인트가 명확하고, 파트너링 스토리를 만들기 쉽습니다. 하지만 동시에 “고위험 자산”으로도 분류되기 쉬워, 해외 파트너나 투자자는 ‘설명 가능한 시스템’을 요구합니다. 그래서 해외 임상은 “국가를 바꿔서 한 번 더 한다”가 아니라, 글로벌 기준으로 읽히는 증거 패키지를 만드는 작업이 됩니다.
실무적으로는 다음 6가지를 “미리 설계된 상태”로 만들어두면 해외 임상과 BD가 동시에 쉬워집니다. 첫째, PD/기전 증거 설계(샘플, 타이밍, 분석 방법). 둘째, 지연·누적 독성을 전제로 한 safety monitoring 구조. 셋째, CMC 일관성과 변경관리의 기본 원칙(브릿징 논리 포함). 넷째, central lab과 샘플 체인의 추적성. 다섯째, EDC–Safety–PK/PD 데이터 정합(reconciliation) 리듬. 여섯째, go/no-go 기준을 다중 지표로 두는 것(ORR 하나로 결론 내리지 않기).
이 여섯 가지는 “문서 늘리기”가 아니라, 나중에 프로그램이 커질 때도 흔들리지 않는 운영 체계를 미리 만들어 두는 겁니다. 실제로 이런 체계가 잡혀 있으면, 다음 프로그램부터 속도가 빨라지고, 파트너가 질문하는 비용도 줄어듭니다.
2026년 이후 ADC의 핵심은 payload의 기전이 될 가능성이 크다
AACR 2026에서 보인 pan-RAS 억제제 페이로드 ADC 사례는, ADC가 단순 세포독성 운반체를 넘어 기전 delivery 플랫폼으로 확장되고 있음을 보여줍니다. 이 변화는 임상 PoC의 모양, 안전성 전략, CMC/변경관리, 데이터 거버넌스까지 함께 바꿉니다. 결국 “무슨 타깃인가”만으로는 부족해지고, “무슨 기전을 싣고 있으며 그 기전을 어떻게 증명하고 통제하는가”가 개발과 파트너링의 핵심 질문이 될 가능성이 큽니다.
인투인월드(Intoinworld)는 한국 현지에서 10년 이상 임상시험을 지원해 온 CRO로서, 1상부터 4상 및 시판 후 조사까지 폭넓은 경험을 보유하고 있습니다. 신규 모달리티(ADC 포함)의 해외 임상 실행을 고려 중이시라면, IND/IRB 대응부터 사이트 운영, 데이터·안전성 운영까지 전 과정을 실무 중심으로 지원해 드립니다. 페이지 내 무료 견적(Quotation) 버튼을 통해 문의해 주세요.



