차세대 세포 치료제 시장의 구조적 진화
지난 10년 동안 키메릭 항원 수용체 T세포(Chimeric Antigen Receptor T-cell, CAR-T) 치료제는 혈액암 치료에 있어 전례 없는 완치율을 기록하며 종양학의 판도를 완전히 뒤바꾸었다. 그러나 현재 상용화된 1세대 CAR-T 치료제는 환자의 혈액에서 T세포를 채취(Leukapheresis)하여 체외(Ex vivo) GMP 제조 시설로 운송한 뒤, 유전자 조작 및 증양을 거쳐 다시 환자에게 주입하는 극도로 복잡하고 다단계적인 생산 공정에 의존하고 있다. 이러한 체외 제조 방식은 필연적으로 3~6주에 달하는 긴 생산 대기 시간(Vein-to-vein time)을 발생시키며, 이 기간 동안 병세가 급격히 악화되는 중증 환자들은 치료의 기회조차 얻지 못하는 실정이다. 또한 1회 투여에 미화 40만~50만 달러를 상회하는 살인적인 제조 원가(COGS)와 광범위한 림프구 고갈 화학요법(Lymphodepleting chemotherapy)의 사전 필수 적용은 기존 CAR-T 치료제의 글로벌 확장성을 심각하게 제한해 왔다.
2026년 현재, 바이오 제약 산업은 이러한 물류적, 재무적, 임상적 한계를 일거에 타파할 ‘인비보(In vivo) CAR-T’ 기술의 상용화 궤도 진입이라는 거대한 패러다임 전환을 목도하고 있다. 인비보 CAR-T는 환자의 신체 외부로 세포를 꺼내지 않고, CAR 유전 암호를 탑재한 전달 벡터(Lentiviral vector, Lipid Nanoparticle 등)를 환자의 체내에 직접 정맥 주사하여 체내의 T세포를 그 자리에서 즉시 CAR-T 세포로 재프로그래밍하는 혁신적인 접근법이다. 이는 세포 치료제를 환자 맞춤형 ‘제조 서비스’ 모델에서 기성품(Off-the-shelf) 형태의 ‘표준 의약품’ 모델로 전환시킴을 의미한다. 제조 모델의 근본적인 변화는 필연적으로 리스크 모델의 변화를 동반하며, 결과적으로 Clinical Trials의 설계, 안전성 모니터링, 데이터 운영 체계 전반에 걸친 전면적인 개편을 요구하고 있다. 본 보고서는 대형 제약사들의 공격적인 M&A 동향, 새롭게 대두되는 Clinical Trials 프로토콜의 난제, 미국 FDA의 규제 완화 조치, 그리고 지정학적 재편에 따른 글로벌 CRO(Contract Research Organization) 운영 전략을 종합적으로 분석하여 2026년 제약·바이오 산업의 핵심 인사이트를 제공한다.
인비보(In Vivo) T세포 엔지니어링의 과학적 기반과 플랫폼 분류
인비보 CAR-T의 성공 여부는 체내에 주입된 유전자 전달 물질이 비표적 세포(Non-target cells)를 회피하고 오직 표적 T세포에만 선택적으로 결합하여 유전자를 발현시키는 ‘표적화(Targeting) 효율성’에 전적으로 달려 있다. 현재 초기 단계 Clinical Trials에서 두각을 나타내고 있는 플랫폼은 크게 바이러스성 벡터(Viral Vectors)와 비바이러스성 벡터(Non-viral Vectors) 두 가지 축으로 양분된다.
바이러스성 벡터 플랫폼: 렌티바이러스(Lentivirus)와 iGPS 기술
렌티바이러스 벡터(LV)는 1세대 체외 CAR-T 제조에서 이미 그 효능과 안전성이 입증된 매개체이나, 체내에 직접 주입할 경우 간(Liver)이나 대식세포(Macrophage) 등 비표적 장기로 유입되거나 무작위적인 유전체 삽입 변이(Insertional mutagenesis)를 유발할 수 있다는 치명적인 단점이 존재했다.
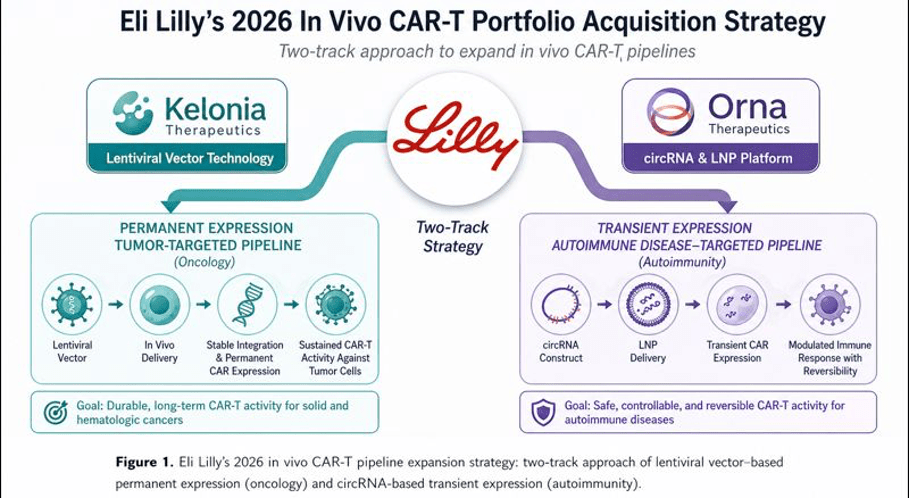
최근 켈로니아 테라퓨틱스(Kelonia Therapeutics)와 같은 선도 기업들은 이러한 한계를 극복하기 위해 바이러스 표면의 외피 당단백질(Envelope glycoprotein)을 정밀하게 개량한 생체 내 유전자 배치 시스템(iGPS®)을 개발하였다. 이 기술은 바이러스 입자가 본래 가지고 있던 감염 지향성(Tropism)을 제거한 뒤, T세포 표면의 특정 마커(예: CD8)에만 결합하도록 항체를 부착하는 방식이다. 이 플랫폼은 유전자를 숙주 세포의 DNA에 영구적으로 통합(Integration)시키므로, 한 번의 주입만으로도 장기적이고 지속적인 항암 면역 반응을 유도할 수 있어 재발성/불응성 다발성 골수종과 같은 공격적인 혈액암 Clinical Trials에서 압도적인 성과를 보이고 있다.
비바이러스성 벡터 플랫폼: 지질 나노입자(LNP)와 원형 RNA(circRNA)
반면, RNA 기반의 지질 나노입자(LNP) 플랫폼은 바이러스성 벡터가 지닌 유전체 통합의 위험성을 원천적으로 배제한 비통합적(Non-integrating) 접근 방식을 취한다. 오르나 테라퓨틱스(Orna Therapeutics)는 선형 mRNA보다 체내 안정성이 뛰어나고 단백질 발현 지속 시간이 긴 독자적인 원형 RNA(Circular RNA, circRNA) 기술을 LNP에 탑재하였다.
LNP를 통한 RNA 전달 방식은 T세포의 유전체를 영구적으로 변형시키지 않고 세포질 내에서 일시적으로만 CAR 단백질을 발현시킨다(Transient expression). 이는 항원 소실이나 T세포 탈진(Exhaustion)을 예방하는 데 유리하며, 특히 자가면역질환(Autoimmune diseases) 치료에 있어 매우 이상적이다. 전신성 홍반성 루푸스(SLE)와 같은 질환의 Clinical Trials에서는 병원성 B세포를 단기간에 일소하여 ‘면역 체계 리셋(Immune reset)’을 유도한 뒤, CAR-T 세포가 자연스럽게 소멸되도록 하는 전략이 요구되기 때문이다. 또한 일시적 발현 모델은 필요 시 반복 투여(Repeat dosing)가 가능하다는 중대한 임상적 이점을 제공한다.
| 평가 지표 | 전통적 체외(Ex Vivo) CAR-T | 바이러스성 인비보 CAR-T (예: Lentivirus) | 비바이러스성 인비보 CAR-T (예: LNP/circRNA) |
| 제조 모델 | 개별 환자 맞춤형 중앙 집중식 제조 | 대량 생산 가능한 기성품(Off-the-shelf) | 대량 생산 가능한 기성품(Off-the-shelf) |
| 치료 소요 시간 | 3~6주 이상 (세포 채취 및 공정) | 수 일 이내 (정맥 주사 직후 체내 발현) | 수 일 이내 (정맥 주사 직후 체내 발현) |
| 전처치 화학요법 | 필수적 (강력한 림프구 고갈 요구) | 일반적으로 불필요 | 불필요 |
| CAR 발현 기간 | 영구적 (유전체 통합) | 영구적 (유전체 통합) | 일시적 (세포질 번역, 수주 내 소멸) |
| 핵심 임상 리스크 | 중증 CRS, ICANS, 제조 실패 및 대기 | 유전체 삽입 변이(Insertional mutagenesis) | 표적 외 기관(간 등) 축적, 반복 투여 필요성 |
| 주요 적응증 | 혈액암 (백혈병, 림프종 등) | 혈액암 및 고형암 (강력한 지속성 요구) | 자가면역질환 및 단기 면역 리셋 요구 질환 |
Table 1: 체외(Ex vivo) CAR-T와 인비보(In vivo) CAR-T 기술 및 벡터별 특성 비교 분석.
2026년 빅파마 M&A 동향: 일라이 릴리(Eli Lilly)의 전방위적 파이프라인 확장
최근 1~2년 사이 인비보 CAR-T 전달 기술이 개념 증명(PoC) 단계를 넘어 본격적인 Clinical Trials 단계로 진입함에 따라, 이 분야를 선점하기 위한 다국적 제약사(Big Pharma)들의 ‘광란의 인수전(Feeding frenzy)’이 전개되고 있다. 특히 대사질환 치료제(Mounjaro, Zepbound)의 천문학적인 매출로 막대한 현금 유동성을 확보한 일라이 릴리(Eli Lilly)는 2026년 상반기에만 두 건의 초대형 인수를 성사시키며 차세대 유전자 의약품 시장의 절대 강자로 부상했다.
- 켈로니아 테라퓨틱스(Kelonia Therapeutics) 70억 달러 인수
2026년 4월 20일, 일라이 릴리는 렌티바이러스 기반 인비보 유전자 전달 플랫폼 선도 기업인 켈로니아 테라퓨틱스를 최대 70억 달러(선급금 32억 5천만 달러, 마일스톤 37억 5천만 달러)에 인수하는 확정적 계약을 발표했다. 켈로니아의 선도 파이프라인인 ‘KLN-1010’은 재발성/불응성 다발성 골수종 환자를 대상으로 BCMA(B-cell maturation antigen) 단백질을 표적하는 1상 Clinical Trials를 진행 중이다.
2025년 ASH(미국혈액학회)에서 발표된 1상 임상 데이터는 시장에 엄청난 파장을 일으켰다. 전처치 화학요법(Lymphodepleting chemotherapy) 없이 KLN-1010을 단회 정맥 주사한 결과, 체내 순환 T세포의 최대 72%가 CAR-T 세포로 성공적으로 전환되었으며, 초기 평가된 4명의 환자 전원(100%)에서 미세잔존질환(MRD) 음성 반응이라는 경이로운 효능이 규명되었다. 더욱이 기존 CAR-T의 치명적 부작용인 3등급 이상의 사이토카인 방출 증후군(CRS)이나 신경독성(Neurotoxicity)이 전혀 보고되지 않아 안전성 측면에서도 획기적인 진전을 이루었다. 릴리는 이번 인수를 통해 엑스비보 CAR-T의 물류적 한계를 우회하고, 복잡한 종양학 Clinical Trials의 패러다임을 바꿀 강력한 영구 발현형 무기를 확보하게 되었다.
오르나 테라퓨틱스(Orna Therapeutics) 24억 달러 인수
종양학 분야에 켈로니아가 있다면, 면역학 및 자가면역질환 분야를 위해서는 오르나 테라퓨틱스가 선택되었다. 2026년 2월, 릴리는 오르나 테라퓨틱스를 최대 24억 달러에 인수했다. 오르나의 핵심 자산인 ‘ORN-252’는 CD19를 표적하는 인비보 CAR-T 치료제로, B세포 구동 자가면역질환 치료를 위해 설계되어 1상 Clinical Trials 진입을 목전에 두고 있다.
오르나의 LNP 및 circRNA 플랫폼은 앞서 언급한 바와 같이 ‘일시적 발현’을 특징으로 한다. 릴리의 면역학 연구 책임자인 프란시스코 라미레즈-발레(Francisco Ramírez-Valle) 박사는 “자가면역질환 환자에게 체외 CAR-T 접근법은 비용과 복잡성 면에서 한계가 명확하다. 오르나의 플랫폼은 병원성 B세포를 리셋하는 동시에 영구적인 유전자 변형의 리스크를 피할 수 있어, 전신성 홍반성 루푸스(SLE) 등 다양한 자가면역질환 Clinical Trials에 이상적이다”라고 평가했다.
업계 내 연쇄 반응과 M&A 파급 효과
릴리의 행보는 고립된 사건이 아니다. 애브비(AbbVie)는 캡스탄 테라퓨틱스(Capstan Therapeutics)를 21억 달러에, BMS는 오르비탈 테라퓨틱스(Orbital Therapeutics)를 15억 달러에, 길리어드(Gilead/Kite)는 인터리우스 바이오테라퓨틱스(Interius BioTherapeutics)를 3억 5천만 달러에 연달아 인수하거나 대규모 파트너십을 체결했다. 피치북(PitchBook)의 분석가 벤 저처(Ben Zercher)에 따르면, 존슨앤드존슨(J&J)이나 노바티스(Novartis)와 같이 아직 인비보 CAR-T 포트폴리오를 확보하지 못한 거대 제약사들이 우모자 바이오파마(Umoja Biopharma) 등 남은 독립 바이오텍을 향해 공격적인 러브콜을 보낼 것으로 전망된다. 이는 곧 향후 수년 내에 글로벌 Clinical Trials 시장에 인비보 세포 치료제 파이프라인이 폭발적으로 유입될 것임을 예고한다.
차세대 Clinical Trials 프로토콜 설계의 난제와 전략
생체 내부를 직접 유전자 조작의 공장으로 활용하는 인비보 CAR-T는 기존 약물 개발의 상식을 파괴한다. 따라서 이러한 신약을 검증하기 위한 Clinical Trials의 설계, 모니터링, 데이터 수집 체계 역시 완전히 새로운 국면을 맞이하고 있다.
바이오마커 기반의 투여량(Dosing) 결정 및 PK/PD 모델링
기존 엑스비보 CAR-T의 Clinical Trials에서는 환자에게 투여할 ‘살아있는 CAR-T 세포의 절대적인 수(예: 1억 개의 세포)’를 명확히 측정하고 용량을 결정할 수 있었다. 반면, 인비보 CAR-T Clinical Trials에서는 투여되는 단위가 세포가 아닌 ‘유전자 전달 벡터의 입자 수(Viral genomes 또는 LNP mass)’이다. 주입된 벡터가 체내에서 얼마나 많은 T세포를 성공적으로 형질전환(Transduction)시킬지, 그리고 그 세포들이 언제 최고조(Peak)로 증식할지는 환자의 면역 생태계에 따라 극심한 편차를 보인다.
따라서 2026년의 선도적인 Clinical Trials 마스터 프로토콜은 단순한 용량 증량(Dose escalation) 규칙을 넘어, 정교한 약동학(PK) 및 약력학(PD) 바이오마커에 의존하고 있다. 연구자들은 액체 생검(Liquid biopsy)과 고해상도 유세포 분석(Flow cytometry)을 통해 체내 벡터의 생체 분포(Biodistribution), 표적 T세포 내 유전자 침투율, CAR 단백질 발현 동태를 실시간으로 추적하며 투여 주기를 유연하게 조정해야 한다.
안전성 제어: On-Target Off-Tumor 독성과 벡터 면역원성
전신 정맥 투여 방식은 안전성 측면에서 치명적인 리스크를 내포하며, 이는 Clinical Trials 수행 시 가장 중점적으로 통제되어야 할 영역이다.
- On-target Off-tumor 독성 및 비표적 침투: LNP나 바이러스 벡터가 의도한 T세포가 아닌 대식세포나 조절 T세포(Tregs)와 같은 억제성 면역 세포에 잘못 침투할 경우, 종양 미세환경(TME) 내의 면역 억제 작용을 오히려 강화하는 치명적인 역효과를 낳을 수 있다. 따라서 임상 설계 시 간독성 지표 및 조직 생검을 통한 벡터의 비표적 장기 축적 여부를 엄격히 평가해야 한다.
- 전달 매개체의 면역원성(Immunogenicity): 환자가 이미 렌티바이러스나 LNP 페길화(PEGylation) 지질에 대한 중화항체를 보유하고 있을 경우, 주입된 벡터가 T세포에 도달하기도 전에 체내 면역계에 의해 파괴될 수 있다. 특히 mRNA 기반 기술에서 효능을 유지하기 위해 약물을 재투여(Re-dosing)해야 할 경우, 항약물항체(ADA) 형성을 방지하기 위한 정밀한 면역 억제 스케줄이 Clinical Trials 프로토콜에 통합되어야 한다.
- 안전성 스위치(Safety Switch)의 도입: 예기치 못한 과도한 사이토카인 방출 증후군(CRS)이나 신경독성을 통제하기 위해, 최신 Clinical Trials에서는 소분자 약물을 투여했을 때만 CAR가 활성화되거나 반대로 자멸(Apoptosis)하도록 설계된 ‘논리 회로(Logic-gated) CAR’ 또는 ‘안전 스위치’ 메커니즘을 필수적으로 탑재하고 있다.
15년 이상의 장기 추적 관찰(LTFU) 인프라 구축
렌티바이러스와 같이 유전체에 통합되는 벡터를 사용하는 인비보 CAR-T 치료제는 삽입 돌연변이에 의한 이차 원발성 악성종양(SPM) 발생 리스크를 완전히 배제할 수 없다. 미국 FDA 및 유럽 EMA의 엄격한 가이드라인에 따라, 임상 스폰서와 CRO는 1차 Clinical Trials가 종료된 이후에도 해당 환자를 최장 15년 동안 추적 관찰(Long-Term Follow-Up, LTFU)해야 하는 막중한 규제적 책임을 진다. 이는 기존의 단기적인 임상 데이터 관리 시스템으로는 감당할 수 없으며, 국제적인 환자 레지스트리 인프라를 활용하여 환자가 임상 기관을 이탈하더라도 지속적인 안전성 데이터를 추출할 수 있는 데이터 정합(Data Integrity) 체계가 확보되어야 한다.
글로벌 규제 프레임워크의 진화: 2026년 미국 FDA CMC 유연성 확대
전례 없는 속도로 발전하는 유전자 의약품 기술에 발맞추어, 규제 당국 역시 혁신적인 치료제가 더 빨리 환자에게 도달할 수 있도록 심사 제도를 개편하고 있다. 과거 엑스비보 세포 치료제 개발사들은 극소수의 환자를 대상으로 하는 1~2상 임상 단계에서도 상업용 의약품 수준의 까다로운 화학·제조·품질관리(CMC) 규정을 충족해야 했으며, 이는 막대한 시간 지연과 자본 고갈의 원인이 되었다.
이러한 병목 현상을 해소하기 위해, 2026년 1월 11일 미국 FDA 산하 생물의약품평가연구센터(CBER)는 세포 및 유전자 치료제(CGT)의 CMC 요건에 대한 전향적인 ‘규제 유연성(Regulatory Flexibility)’ 가이드라인을 전격 발표했다. 마티 마카리(Marty Makary) FDA 국장은 “세포 및 유전자 치료제의 고유한 특성을 반영한 상식적인 개혁을 통해 규제 장벽을 낮추고 혁신을 촉진하겠다”고 천명했다.
새로운 가이드라인에 따라, 인비보 CAR-T 파이프라인을 보유한 바이오텍들은 2상 및 3상 Clinical Trials를 위한 임상용 의약품 제조 시 기존의 엄격한 21 CFR part 211 규정을 완벽히 준수하지 않아도 되는 예외(210.2(c))를 적용받게 된다. 또한, 후기 Clinical Trials로 진입하는 과정에서 벡터의 성분이나 정제 공정에 사소한 변경이 발생하더라도, 광범위한 재검증이나 임상 지연 없이 제한적인 동등성 데이터(Comparability data)만으로 공정 변경을 승인받을 수 있게 되었다. 이러한 규제 패러다임의 혁신은 초기 발견 단계의 유망한 인비보 CAR-T 물질들이 후기 Clinical Trials를 거쳐 상업화에 이르는 기간을 수년 이상 파격적으로 단축시킬 것으로 전망된다.
| 규제 및 검증 영역 | 기존 FDA CMC 요구 사항 | 2026년 신규 FDA 규제 유연성 (가이드라인 적용) |
| 임상 2상/3상 제조 규정 | 상업용에 준하는 21 CFR part 211 전면 준수 | 21 CFR 210.2(c)에 따른 광범위한 예외 인정 및 유연성 부여 |
| 의약품 출하(Release) 기준 | 임상 초기부터 엄격하게 확립된 최종 규격 요구 | 임상 시험 단계에 부합하는 허용적(Permissive) 출하 기준 인정 |
| 공정 및 제조 변경(Changes) | 대규모의 시간과 자본이 소요되는 동등성 입증 | 가벼운 변경에 대해 간소화된 데이터 제출로 신속한 승인 허용 |
| 제품 수명주기 접근법 | 초기 확립된 스펙의 영구적 고정 요구 | 임상 진행 데이터에 따른 스펙의 점진적 최적화(Refinement) 허용 |
Table 2: 2026년 세포·유전자 치료제(CGT) 승인 가속화를 위한 미국 FDA CMC 규제 유연성 가이드라인 요약.
생물보안법(BIOSECURE Act) 발효와 Clinical Trials 공급망의 지정학적 재편
임상 과학과 규제 당국의 노력 외에도, 2026년 글로벌 바이오 제약 산업을 덮친 가장 거대한 거시적 변수는 지정학적 안보 위기에서 비롯되었다. 2025년 말 미국 의회를 통과하여 2026년부터 본격적인 효력을 발휘하기 시작한 ‘생물보안법(BIOSECURE Act)’은 글로벌 Clinical Trials의 아웃소싱 및 데이터 라우팅 지형을 송두리째 흔들어 놓았다.
생물보안법의 핵심 골자는 미국 연방 자금을 지원받거나 연방 정부와 계약을 맺는 모든 기관 및 기업이 ‘외국의 적대 세력(Foreign adversaries)’과 연계된 우려 바이오테크 기업(Biotechnology companies of concern)의 장비, 서비스, 데이터를 사용하는 것을 엄격히 금지하는 것이다. 특히 미국 하원 중국특위는 일부 중국 국방부(PLA) 산하 군 병원 및 의료 기관들이 서방 제약사들의 Clinical Trials에 조직적으로 개입하여 미국 시민의 민감한 유전체 및 다중오믹스(Multiomic) 데이터를 무단으로 수집하고 군사적 또는 상업적 목적으로 전용할 수 있다는 짙은 우려를 표명하였다.
인비보 CAR-T 치료제의 경우, 환자의 면역 프로파일링과 유전자 서열 분석, 바이오마커 추적이 임상 데이터의 핵심을 이룬다. 따라서 다수의 글로벌 제약사들은 중국 기반의 CDMO(위탁개발생산) 업체나 임상 수탁 기관과의 기존 계약을 파기하고, 2026년을 기점으로 자사의 혁신적인 유전자 의약품 파이프라인을 완전히 새롭고 안전한 권역으로 이전(Decoupling)해야만 하는 절체절명의 과제에 직면하게 되었다. 이는 단순히 임상 장소를 옮기는 문제를 넘어, 환자 데이터 보안성, 윤리적 임상 수행 기준(ICH GCP), 그리고 현지의 첨단 의료 인프라 수준을 엄격하게 재평가하는 글로벌 엑소더스를 촉발하였다.
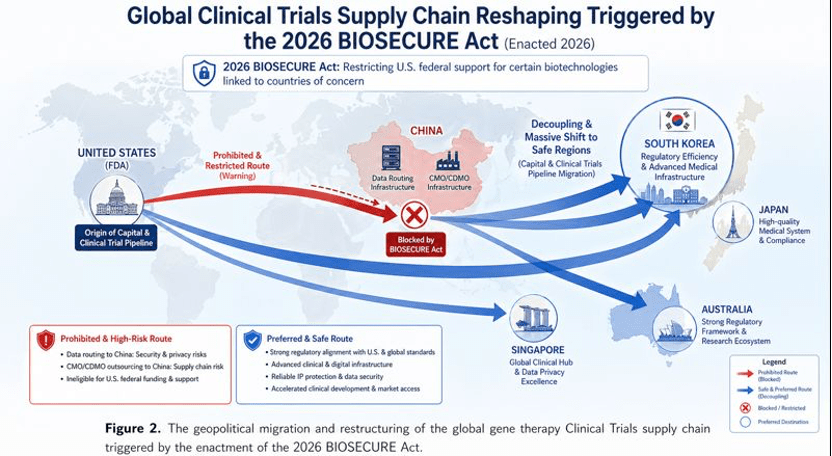
아시아 태평양의 허브: 한국(South Korea)의 Clinical Trials 경쟁력과 글로벌 CRO 전략
생물보안법으로 인한 글로벌 공급망 재편의 최대 수혜 지역이자, 차세대 인비보 CAR-T 개발의 이상적인 테스트베드로 대한민국(South Korea)이 확고히 부상하고 있다. 고도로 고도화된 의료 인프라, 전 국민 건강보험 체계를 바탕으로 한 방대한 환자 코호트, 그리고 글로벌 수준의 임상 규제 준수율은 한국을 전 세계 4~5위권의 Clinical Trials 강국으로 끌어올렸다. 글로벌 제약사와 바이오텍이 한국 시장을 최우선으로 고려하는 이유는 명확하다.
초고속 임상 진입을 가능케 하는 압도적인 규제 효율성
혁신 신약 개발에서 ‘시간(Time to Market)’은 곧 생존과 직결된다. 글로벌 경쟁이 치열한 인비보 CAR-T 분야에서 초기 환자 데이터를 선점하는 것은 막대한 가치를 창출한다. 한국의 규제 당국인 식품의약품안전처(MFDS)는 글로벌 최고 수준의 전문성을 갖춘 리뷰 심사관들을 배치하고 있으며, 임상시험계획(IND) 승인까지 소요되는 기간은 평균 30일(근무일 기준)에 불과하다.
무엇보다 강력한 이점은 MFDS의 행정적 IND 심사와 각 임상 실시 기관(병원)의 윤리위원회(IRB) 심사를 병렬적(Parallel)으로 진행할 수 있다는 점이다. 서방 국가나 타 아시아 국가들이 순차적 심사로 인해 임상 준비에 수개월 이상이 소요되는 반면, 한국에서는 최상의 시나리오에서 제출 후 단 6~8주 만에 첫 환자 투여(First-Patient-In, FPI)가 가능할 정도로 압도적인 속도를 자랑한다. 초기 임상 개발 및 규제 승인 단축에 대한 심층 분석은 https://intoinworld.com/korea-clinical-trials-phase-i-ii-strategy/ 에서 제공하는 자료를 참조할수 있다.
최고 수준의 연구 인프라와 환자 밀집도
한국의 수도 서울(Seoul)은 단일 도시 기준으로 전 세계에서 가장 많은 수의 Clinical Trials가 수행되는 메가 허브이다. 5,100만 명의 인구 중 절반에 가까운 수가 수도권에 밀집해 있으며, 이 지역에는 최첨단 설비와 연구진을 갖춘 대형 3차 대학 병원들이 거대한 클러스터를 형성하고 있다.
일례로 서울대학교병원(SNUH)의 경우 2015년부터 2020년 사이에만 무려 945건의 초기 항암제 Clinical Trials를 성공적으로 수행한 이력을 보유하고 있다. 이 병원은 환자의 유전체 분석을 통한 임상 설계 최적화를 위해 KMed.AI와 같은 독자적인 대규모 언어 모델(LLM)과 임상 의사 결정 지원 시스템(CDSS)을 운영하고 있으며, 병원 내부에 세포 치료제 생산을 위한 GMP 시설을 완비하여 기초 연구부터 환자 투여에 이르는 즉각적인 중개 연구(Translational research) 생태계를 구축하고 있다. 인비보 CAR-T와 같이 임상 프로토콜이 복잡하고 예기치 못한 중증 면역 독성(CRS, 신경독성 등)에 대한 24시간/주 7일 실시간 응급 대응과 집중 치료실(ICU) 연계가 필수적인 초기 임상 단계에서, 한국 병원들의 우수한 의료 인력과 대응 능력은 스폰서에게 비교 불가능한 신뢰를 제공한다.
글로벌 CRO 기반의 통합 임상 운영 시스템 (Clinical Trials as an Operating System)
한국에서의 임상 성공은 단순히 인프라가 존재한다는 사실만으로 보장되지 않는다. 현지의 엄격한 규제 프레임워크를 조율하고, 복잡한 인비보 CAR-T Clinical Trials의 병원 간 물류 및 데이터 정합성을 관리하며, 글로벌 스탠다드(ICH GCP)에 완벽히 부합하는 증거 패키지(Evidence Package)를 생산해 낼 수 있는 ‘현지 전문성을 갖춘 글로벌 CRO’와의 전략적 파트너십이 절대적으로 요구된다.
현대의 CRO는 단순한 행정 대행업체를 넘어 Clinical Trials 전체의 사이클을 통합 관리하는 하나의 거대한 ‘운영 시스템(Operating System)’으로 진화하였다. 고도로 숙련된 한국의 CRA(임상시험모니터요원) 및 CRC(임상시험코디네이터) 조직은 스폰서를 대리하여 각 센터의 윤리 기준 준수 여부를 밀착 감독하며, 실시간 데이터 캡처를 통해 미국 FDA 및 유럽 EMA의 엄격한 교차 검증 요구를 한 치의 오차 없이 충족시킨다. 성공적인 아시아 태평양 지역 진출을 위한 전략적 지침은 https://intoinworld.com/south-korea-clinical-trials-powerhouse/ 페이지에서 상세히 확인할 수 있다.
| 핵심 지표 | 대한민국(South Korea) 임상 경쟁력 수치 | 글로벌 임상 스폰서 이점 |
| 초기 준비 기간(Start-up) | 평균 6주 ~ 8주 (IND / IRB 병렬 심사) | 타 국가 대비 수개월 단축, 특허 기간 최적화 확보 |
| 규제당국 IND 심사 소요 | 약 30 근무일 (사전 상담을 통한 단축 가능) | 투명하고 예측 가능한 마일스톤 설계 |
| 글로벌 임상 점유율 | 전 세계 국가 순위 Top 4~5위 (2023년 9% 성장) | 풍부한 피험자 풀 및 검증된 모집 속도 |
| 인프라 밀집도 | 수도권 내 100여 개 이상의 식약처 인증 대형 병원 | 신속하고 효율적인 다기관(Multi-center) 임상 전개 |
| 데이터 신뢰도 | ICH GCP 완전 준수 및 WHO 평가 최우수 등급 | FDA, EMA 신약 허가 제출 시 무결성 데이터로 100% 인정 |
Table 3: 생물보안법 이후 글로벌 스폰서들이 주목하는 한국(South Korea)의 Clinical Trials 환경 분석 지표.
유전자 의약품 혁명의 완성
인비보(In vivo) CAR-T 기술은 지난 수십 년간 엑스비보 세포 치료제가 넘지 못했던 물류의 장벽, 생산의 실패, 그리고 천문학적인 비용의 한계를 혁신적으로 붕괴시키고 있다. 일라이 릴리가 주도한 켈로니아와 오르나의 2026년 대규모 연쇄 인수는 바이러스성 렌티바이러스 기반의 ‘영구 발현형 종양 타깃 파이프라인’과 LNP 및 원형 RNA(circRNA) 기반의 ‘일시 발현형 자가면역질환 파이프라인’ 양축이 상업적 검증의 문턱을 넘었음을 전 세계에 선포한 사건이다. 이는 향후 모든 면역학 및 종양학 약물 파이프라인이 환자의 몸을 공장으로 사용하는 직접 유전자 편집 방식으로 수렴할 것임을 강하게 시사한다.
그러나 전달 기술의 고도화는 필연적으로 완전히 새로운 차원의 리스크 관리 모델을 동반한다. 2026년의 임상 스폰서들은 체내 유전자 발현을 실시간으로 추적하는 바이오마커 발굴, On-target off-tumor 독성 및 신경독성의 철저한 모니터링, 그리고 15년에 이르는 장기 추적 관찰(LTFU) 시스템이라는 난해한 프로토콜을 정밀하게 통제해야만 한다. 여기에 더해 FDA의 CMC 규제 유연화와 생물보안법(BIOSECURE Act) 발효라는 제도적, 지정학적 대격변은 신약 개발의 무대를 근본적으로 재편하고 있다.
이러한 복합적인 불확실성의 시대에, 글로벌 스폰서들이 취할 수 있는 유일한 생존 전략은 ‘속도’와 ‘데이터 무결성’을 동시에 담보할 수 있는 최상위 임상 허브로 자본을 이동시키는 것이다. 빠르고 유연한 규제 심사, 초고밀도의 첨단 의료 인프라, 그리고 고도로 전문화된 글로벌 CRO 운영 시스템을 통합적으로 제공하는 대한민국(South Korea)은, 차세대 인비보 CAR-T Clinical Trials를 성공적으로 완수하고 전 세계 환자들에게 혁신 신약을 가장 빠르게 공급하기 위한 가장 확실하고 매력적인 전략적 거점임이 분명하다.
귀사의 혁신적인 인비보 CAR-T 파이프라인, 임상 설계부터 막막하십니까?
차세대 세포·유전자 치료제의 복잡한 바이오마커 설계, 엄격한 장기 추적 관찰, 그리고 급변하는 글로벌 규제 프레임워크를 완벽하게 통제할 수 있는 파트너가 필요합니다. 세계 최고 수준의 임상 인프라를 갖춘 한국 시장에서, 6~8주 만에 임상 진입(FPI)을 가능케 하는 압도적인 속도를 직접 경험해 보십시오.
글로벌 제약·바이오 산업의 핵심 트렌드를 가장 먼저 확인하세요!
FDA의 최신 규제 유연성 정책, 빅파마의 최신 M&A 동향, 그리고 아시아 태평양 지역의 임상 인프라 진화에 대한 딥다이브 리포트를 놓치지 마십시오. 글로벌 스폰서와 전문가들이 구독하는 프리미엄 인사이트를 귀하의 메일함으로 직접 전달해 드립니다.
자주 묻는 질문 (FAQs)
Q1. 기존의 체외(Ex vivo) CAR-T와 비교할 때, 인비보(In vivo) CAR-T Clinical Trials의 가장 큰 구조적 차이점은 무엇인가?
A1. 기존 체외 CAR-T는 환자의 혈액을 외부로 반출하여 GMP 공장에서 수 주에 걸쳐 유전자를 조작해야 하므로 제조 지연 및 실패 리스크가 매우 컸다. 반면, 인비보 CAR-T는 체내로 유전자 전달 벡터(LNP 또는 렌티바이러스)를 직접 주사하여 환자의 신체 내부를 치료제 공장으로 활용한다. 따라서 Clinical Trials 진행 시 복잡한 물류 이송이나 입원 전처치 화학요법 없이, 표준화된 기성품(Off-the-shelf) 약물처럼 신속한 투여가 가능하여 임상 속도와 확장성이 극적으로 향상된다.
Q2. 일라이 릴리(Eli Lilly)가 2026년에 켈로니아와 오르나를 동시에 확정 인수한 전략적 배경은 무엇으로 분석되는가?
A2. 일라이 릴리는 인비보 세포 치료제 시장의 두 가지 상이한 기술적 수요를 완벽히 선점하기 위해 투트랙 인수를 단행했다. 켈로니아(약 70억 달러)는 렌티바이러스 벡터 기반으로 유전자를 표적 세포에 영구 통합시키므로 강력하고 지속적인 효과가 필요한 ‘혈액암 및 고형암’ 치료에 적합하다. 반면 오르나(약 24억 달러)는 원형 RNA(circRNA)와 LNP를 결합하여 체내에서 일시적으로만 CAR 단백질을 발현시키므로, 면역 체계의 리셋이 필요한 전신성 홍반성 루푸스(SLE) 등 ‘자가면역질환’ Clinical Trials에 가장 이상적인 안전성을 제공한다.
Q3. 인비보 CAR-T Clinical Trials 설계 시 가장 중점적으로 모니터링해야 할 임상적 안전성 리스크는 무엇인가?
A3. 환자 체내로 강력한 유전자 조작 물질을 직접 주입하므로 ‘On-target Off-tumor’ 독성, 즉 벡터가 표적 T세포가 아닌 대식세포나 간 조직 등 엉뚱한 장기로 유입되어 문제를 일으키는지 정밀하게 관찰해야 한다. 또한 바이러스성 벡터를 사용할 경우 환자 본연의 중화항체에 의한 즉각적인 면역원성 반응이나, 유전체 삽입 변이(Insertional mutagenesis)로 인한 이차 암 발생 우려가 있으므로 이를 감시하기 위한 최장 15년 이상의 장기 추적 관찰(LTFU) 프로토콜이 필수적으로 수반되어야 한다.
Q4. 2026년 미국 FDA가 발표한 세포·유전자 치료제(CGT) CMC 규제 유연성 정책은 임상 개발에 어떠한 영향을 미치는가?
A4. 해당 조치는 기존 규제 당국의 경직된 태도를 탈피한 혁신적 변화이다. FDA는 2상 및 3상 Clinical Trials 진입을 위해 상업용 의약품 수준의 까다로운 제조 규정(21 CFR part 211) 준수 요건을 면제해 주었으며, 임상 진행 중 제조 공정(지질 변경 등)이 소폭 변경되더라도 간소화된 동등성 데이터만으로 승인받을 수 있도록 허용했다. 이로써 인비보 CAR-T 파이프라인의 상업화 소요 기간과 R&D 지출이 획기적으로 감축될 것으로 확신한다.
Q5. 생물보안법(BIOSECURE Act) 발효 이후 한국(South Korea)이 글로벌 Clinical Trials의 핵심 허브로 지목받는 핵심적인 이유는 무엇인가?
A5. 미국 생물보안법에 의해 중국 내 임상 아웃소싱 및 다중오믹스 데이터 공유가 사실상 제한되면서 글로벌 스폰서들은 안전하고 고도화된 대체지를 필사적으로 찾고 있다. 한국은 FDA와 EMA가 100% 신뢰하는 고품질의 임상 데이터 무결성을 보장하며, 식약처(MFDS) 규제 심사와 각 병원 윤리위원회(IRB) 심사가 병렬로 진행되어 제출 후 단 6~8주 만에 임상을 개시(Start-up)할 수 있는 세계 최고 수준의 효율성을 갖추고 있기 때문에, 복잡한 1/2상 Clinical Trials를 수행하기 위한 최적의 생태계로 평가받고 있다.



