2026年的临床试验日益被视为一种系统:评估标准不仅在于是否对中心进行了监查,更在于质量是否源于设计(QbD)、风险是否得到了比例化管理,以及计算机化系统是否端到端地保护了数据完整性。
从实际操作层面看,这要求临床试验领导力从“执行规模”转向治理:申办方、CRO、研究中心和供应商之间职责明确;决策可追溯;且 KPI 是触发行动的客观指标,而非仅仅用于美化仪表盘。
混合型和远程(去中心化)元素目前已成为临床试验的主流,但前提是方案中明确规定了远程模式、变异控制和安全性流程;监管机构认为,只要预先设计好监督机制和数据完整性,去中心化元素在相同的监管要求下是可接受的。
欧洲增加了独特的运营压力:临床试验的提交和维护均通过统一系统(CTIS)进行,且具有明确的最长时限和“停钟”机制;此外,对于在2025年1月31日后继续进行的试验,有明确的过渡要求。
韩国作为多国临床试验的高效节点,其优势建立在并行审查和运营准备的刻意设计之上(监管和 IRB 时限已在国家材料中说明),但“快速审批”无法弥补文件一致性差或供应商/系统准备延迟带来的损失。
放射性药物与诊疗一体化(Theranostics)临床试验是一项特殊的压力测试:半衰期驱动的物流、影像标准化和可追溯性,使得试验表现与受控的时间表及数据血统密不可分。
治理先行:现代 GCP 对临床试验的新要求
2026年临床试验最重大的变化不是某种新工具,而是新的检查逻辑。其基石是国际人用药品注册技术协调会(ICH)于2025年1月6日采纳的 ICH E6(R3) 第三版 Step 4 最终稿。该指南将申办方的责任框架围绕临床试验全生命周期的质量管理和风险比例化控制展开。
这一治理立场与 ICH E8(R1) 紧密结合,后者将“将质量设计到研究中”正式化,要求前瞻性地识别关键质量因素(CtQ)——即那些一旦失效最可能威胁受试者保护或结果可靠性的方面。
分析的防御性同样需要前置:ICH E9(R1) 中的估计标的(Estimand)框架要求在首例受试者入组前,明确目标、伴随事件与缺失数据处理之间的对齐——确保试验的效应估计值具有可解释性且达到决策级别。
对于运营团队,这些原则转化为一条能够经受住发表、检查和内部治理审查的临床试验“证据脊柱”:
第一,构建方案特定的 CtQ 地图与比例化风险计划:定义 (a) 哪些因素会实质性损害受试者或削弱主要结果,(b) 采取何种控制措施防止损害,以及 (c) 哪些信号能证明控制措施有效。
第二,将计算机化系统作为单一证据链进行治理:ICH E6(R3) 描述了用户管理和权限控制。对于闭环系统,电子记录控制包括安全的、计算机生成的、带有时间戳的审计追踪(Audit Trails),以独立记录创建、修改或删除记录的操作,且不掩盖先前的信息。
第三,将供应商监督视为可审计的接口:包括职责、升級标准、决策权和随访证据。当临床试验由多个服务商执行时,这些“接口”往往是检查发现聚集的地方。
从设计到全球交付:工程化临床试验的速度与信任
临床试验表现通常被描述为入组速度,但许多高成本失败始于接口失效:入选标准假设与真实患者不符、方案复杂性导致数据缺失、供应商工作流碎片化导致追溯性断裂。
2026年的运营方法将临床试验的每个领域视为一个工程化子系统,具有明确的容差、负责人和可衡量的产出。
设计选择应回溯至决策问题:正在估计什么效应?在何种伴随事件下?运营容差是多少?狭窄的访视窗口和高受试者负担会推高方案偏离(PD)和数据缺失,动摇分析基础。
运营在临床试验中不再等同于频繁的现场监查。现代预期强调比例化监督,将中心化信号和针对性随访与关键质量因素(CtQ)相对应。
启动(Start-up)是一种治理产物。韩国指南强调,启动时钟包括可行性研究、IND/IRB 准备、合同签署、系统设置和中心激活;只有当准备工作并行完成时,“并行审查”才能带来速度。
患者招募依然是最大的瓶颈。运营上,招募应作为一个受控漏斗进行管理——从首例受试者入组时间、筛选周期、筛选失败率到随访完成率——并与可控杠杆(预筛选逻辑、负担减轻、中心激活纪律)挂钩。
虚拟与混合临床试验现在已是常态:电信医疗、家庭护理和远程数据获取在变异受控且流程明确时是可接受的。监管观点很明确:去中心化元素不会减轻申办方责任,反而增加了必须治理的接口(培训、监督、隐私和源数据定义)。
数据完整性是连接组织。行业评估继续将电子数据采集(EDC)视为核心平台。在合规层面,团队必须能解释为何电子记录是可信的(审计追踪、访问限制)。在互操作性层面,运营风险在于对账延迟(EDC ↔ 实验室 ↔ 影像 ↔ 安全性),因为延迟会推迟数据库锁定和分析里程碑。
在2026年,临床试验中的“风险管理”不是一张幻灯片,而是一个闭环:识别风险、实施控制、监测信号、记录行动。一个高效的纪律是预设必须升级的“红旗信号”(如重复发生的关键偏离、审计追踪异常、系统性中心表现下滑),并将每个信号连接到预先商定的行动。
放射性药物与诊疗一体化临床试验放大了一个事实:如果时间安排出现偏差,质量和数据就会随之崩塌。申办方应在首例患者入组(FPI)前确认:中心是否有核医学资质?供应与进口如何管理?影像读片标准和 QC 如何治理?给药日流程是否明确?对账由谁负责?
区域现实核查:美国、欧盟、韩国与亚太
当临床试验策略被写成带有门户(Gates)的时间表,而非充满愿景的叙事时,它才具备可信度。
在美国,IND 申请通常在药监部门收到后 30 天自动生效(除非收到暂停通知)。对于混合型试验,去中心化元素需明确规定并受控。
在欧盟,临床试验法规(CTR)允许通过 CTIS 进行单一申请,并由成员国协作评估。自 2025 年 1 月 31 日起,所有持续进行的试验都必须符合新规。
在韩国,MFDS 的审查基准约为 30 个工作日,IRB 审查通常并行开展。韩国临床中心(如峨山医疗中心、首尔大学医院)的高患者通量和成熟的 EMR 生态系统可显著加速试验。
在亚太其他地区,中国 NMPA 提供 60 天的“默示许可”路径;日本 PMDA 要求在计划开始前 31 天以上提交临床试验通知;澳大利亚则在放射性药物临床试验中作为重要的补充中心。
战略意义:在各区域保持科学问题和数据治理标准的一致性,同时灵活调整运营接口(工作流、语言、物流),确保临床试验的证据故事不因区域差异而碎片化。
临床试验规划工具表
以下表格将现代临床试验的预期(质量源于设计、基于风险的质量管理、去中心化元素治理以及区域特定的启动时钟)转化为实际的规划工具。这些内容综合了 ICH E6(R3)/E8(R1)/E9(R1)、FDA 去中心化元素指南、欧盟 CTR/CTIS 运营框架、KoNECT 时间线摘要以及 Intoinworld 发布的 2026 年 CRO 运营笔记。
表 1. 临床试验运营模式的权衡(成本、时间线、风险)
| 流程板块 | 规模化前需锁定的产出 | 典型主要负责人 | 需保存供检查/发表的证据 | 需监测的失败信号 |
| 方案意图与估计标对齐 | 估计标说明;伴随事件策略;终点容差和窗口 | 申办方 + 生物统计(CRO 提供建议) | 决策依据;版本控制;可追溯至方案的分析假设 | 方案修订压力;终点模糊;数据缺失风险上升 |
| CtQ 与 RBQM 设计 | CtQ 地图;风险登记表;阈值和触发器;升级路径 | 申办方(负责) + CRO(运营设计) | 风险审查频率;行动日志;CAPA 关联 | 重复的关键偏离;未解决的中心信号;循环发生的根本原因 |
| 启动就绪 | 对齐的国家申报包;翻译词彙表;中心激活清单;供应商计划 | CRO 启动负责人 + 申办方监督 | 提交对齐表;培训完成情况;系统访问控制 | 合同/预算反复磨合;翻译多次修改;供应商入驻拖延 |
| 数据与系统治理 | 数据管理计划;逻辑检查;对账计划;审计追踪计划;变更控制计划 | CRO 数据管理 + 申办方 QMS | 验证状态概覽;用户角色/访问权限;审计追踪审查记录 | 质疑处理老化;对账滞后;无法解释的系统变更 |
| 执行与监督 | 监查计划;中心化监查信号;问题管理 SOP | CRO 临床运营 + 申办方医学监督 | 授权日志;访视模式可追溯性;问题→CAPA 证据 | 问题关闭缓慢;CAPA 后重复发生 |
| 结束与报告 | 数据库锁定标准;CSR 叙述控制;TMF 质量控制结项 | 申办方 + CRO(撰写/运营) | 锁定清单;数据血统;叙述一致性检查 | 锁定后返工;缺失关键文件 |
表 2. 经得起检查的临床试验证据脊柱(流程 + 所有权)
| KPI 领域 | KPI(示例) | 运营定义 | 触发行动(举例) | 证明控制的第一线行动 |
| 速度 | 中心激活周期时间 | 最终申报包 → 中心激活 | 与中心队列相比的离群值;合同导致的重复停顿 | 解决合同模板瓶颈;完善就绪清单;重新基准化关键路径 |
| 招募 | 首例受试者入组时间 | 中心激活 → 首例受試者 | 超出计划的“沉默中心”期 | 激活救援访视;PI/CRC 工作流检查;更新招募材料 |
| 招募质量 | 筛选失败率 | 已筛选 / 已随机化 | 方案变更后无法解释的趋势漂移 | 重新培训 I/E 判定;调整预筛选;尽可能减轻访视负担 |
| 数据质量 | CtQ 缺失数据率 | 访视中缺失的 CtQ 字段 | 某中心/模式呈上升趋势 | 针对性监查;工作流再培训;加强逻辑检查和提醒 |
| 数据速度 | 质疑周期时间 | 质疑开启 → 已解决 | 超过预定限制的老化 | 中心辅导;执行质疑处理纪律;自动升级 |
| 安全性 | SAE 随访及时性 | 初始 SAE → 完成随访 | 重复发生的随访延迟 | 强化升级机制;每周核对安全性与 EDC;调整人员配置 |
| 系统治理 | 审计追踪异常 | 无法解释的配置/用户操作 | 任何无法解释的管理端变更(高关键度) | 冻结配置;调查;CAPA;收紧访问模型和定期审查 |
| 集成 | 对账滞后 | 实验室/影像/安全性 vs EDC | 滞后威胁到中期锁定或数据库锁定 | 增加频率;修复接口;指定单一对账负责人 |
表 3. 临床试验 KPI 仪表盘(KPI → 触发器 → 行动)
| KPI 领域 | KPI(示例) | 运营定义 | 触发行动(举例) | 证明控制的第一线行动 |
| 速度 | 中心激活周期时间 | 最终申报包 → 中心激活 | 与中心队列相比的离群值;合同导致的重复停顿 | 解决合同模板瓶颈;完善就绪清单;重新基准化关键路径 |
| 招募 | 首例受试者入组时间 | 中心激活 → 首例受試者 | 超出计划的“沉默中心”期 | 激活救援访视;PI/CRC 工作流检查;更新招募材料 |
| 招募质量 | 筛选失败率 | 已筛选 / 已随机化 | 方案变更后无法解释的趋势漂移 | 重新培训 I/E 判定;调整预筛选;尽可能减轻访视负担 |
| 数据质量 | CtQ 缺失数据率 | 访视中缺失的 CtQ 字段 | 某中心/模式呈上升趋势 | 针对性监查;工作流再培训;加强逻辑检查和提醒 |
| 数据速度 | 质疑周期时间 | 质疑开启 → 已解决 | 超过预定限制的老化 | 中心辅导;执行质疑处理纪律;自动升级 |
| 安全性 | SAE 随访及时性 | 初始 SAE → 完成随访 | 重复发生的随访延迟 | 强化升级机制;每周核对安全性与 EDC;调整人员配置 |
| 系统治理 | 审计追踪异常 | 无法解释的配置/用户操作 | 任何无法解释的管理端变更(高关键度) | 冻结配置;调查;CAPA;收紧访问模型和定期审查 |
| 集成 | 对账滞后 | 实验室/影像/安全性 vs EDC | 滞后威胁到中期锁定或数据库锁定 | 增加频率;修复接口;指定单一对账负责人 |
表 4. 临床试验各区域的摩擦点(哪些会变,哪些绝不能变)
| 区域 | 主要门户 | 公开说明的规划时钟 | 实际路径中常见的减速因素 | 全球团队的规划响应 |
| 美国 | IND 生效 + IRB | 除非被要求临床暂停,否则在收到后 30 天生效 | 合同、中心工作量、供应商设置 | 构建 Day-0 申报包;预先规划监督和数据工作流 |
| 欧盟 | 通过 CTIS 提交 CTA | 验证/评估/决策的固定最长期限;RFI 的停钟机制 | 第一/第二部分案卷不一致;变更控制;CTIS 数据纪律 | 预先对齐文件;将 CTIS 元数据视为核心交付物 |
| 韩国 | MFDS + IRB(通常并行) | MFDS 约 30 工作日;IRB 约数周(通常并行) | 文件对齐问题、翻译、供应商验证、药品进口/标签 | “首轮提交质量”;仅在准备就绪时并行推进 |
| 中国 | NMPA/CDE 路径 | 60 天决策窗口,无通知则“默示许可” | 本地文件、伦理节拍、问答周期 | 保持科学定义恒定;本地化工作流/语言 |
| 日本 | CTN 预启动窗口 | 初始 CTN 在计划开始前 >31 天提交 | 本地语言/文件;咨询节拍 | 尽早计划本地化;锁定方案意图和容差 |
图示说明
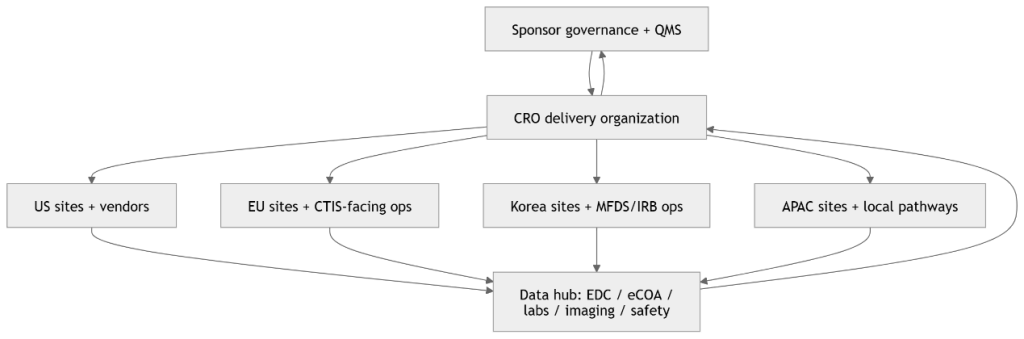
图 1(流程图):从方案意图到临床研究报告(CSR)的临床试验证据脊柱。一个以前瞻性治理为核心的临床试验“操作系统”视图,将设计、执行和报告对齐到单一证据链中。

图 2(临床试验阶段流程 + 时间线):影响首例患者入组的区域感知启动时钟
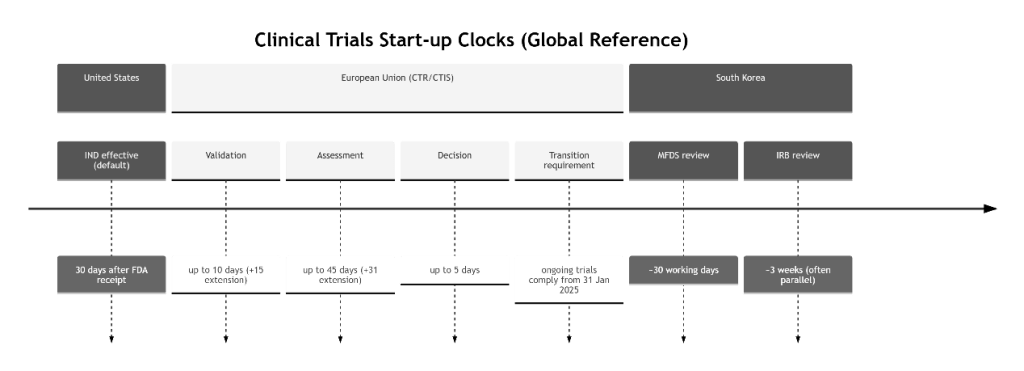
图 3(全球 CRO 网络图):作为受控网络的跨区域临床试验执行