바이오 산업에서 AI 도입은 파일럿을 넘어 운영 성과로 연결되기 시작했다. 2026년의 경쟁력은 ‘가장 큰 모델’을 보유했는가가 아니라, 모델 기반 의사결정을 검증하고 거버넌스로 통제하며 R&D 전반에 확장할 수 있는가에 달려 있다. 본 글은 AI가 실질적 레버리지를 만드는 지점, 운영 모델 변화, 규제기관이 요구하는 신뢰성(credibility)의 방향, 그리고 스폰서가 CRO와 함께 감사 대응성을 유지하며 AI를 운영화하는 방법을 정리한다.
1. 변화의 본질: ‘실험 우선’에서 ‘모델 기반 의사결정’으로 이동한다
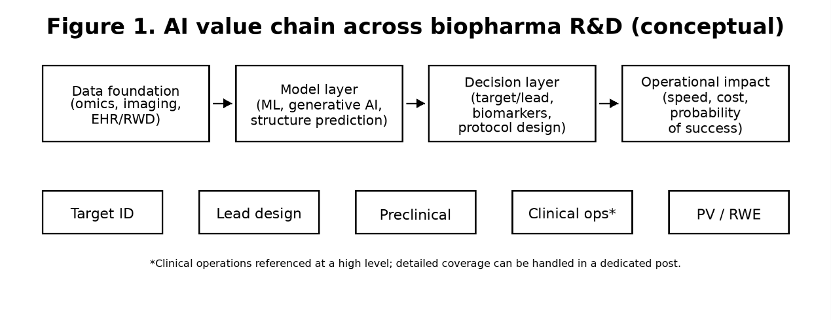
실무에서 관찰되는 변화는 단순하다. AI가 인사이트를 만들 수 있는지보다, 그 인사이트가 실제 검증을 통과하고 의사결정의 품질을 높이는지가 중요해졌다. 초기 성과가 큰 영역은 반복적이고 데이터가 풍부하지만 느렸던 의사결정이다. 예를 들면 타겟 트리아지, 히트 엔리치먼트, 바이오마커 탐색, 문서 중심의 근거 생성 업무가 이에 해당한다.
속도가 한계가 아니라 검증과 거버넌스가 병목이 된다. 모델이 홀드아웃 데이터에서 전향적으로 테스트되지 않거나, 규제 환경에서 감사 가능한 수준으로 설명·추적이 되지 않으면, 해당 모델은 의사결정에 들어오는 순간 가치가 무너진다.
| 의사결정 | AI 접근 | 실무 검증 신호 | 주요 리스크 |
| 타겟 우선순위 | 멀티오믹스 ML + NLP | 홀드아웃 코호트에서 전향적 테스트 | 데이터 누수 / 코호트 편향 |
| 히트-리드 | 인실리코 스크리닝; 생성형 설계 | 실험 확인율(엔리치먼트) | 개발가능성 미반영 |
| 바이오마커 | 클러스터링; 표현학습 | 기관·플랫폼 간 재현성 | 배치 효과를 생물학으로 오인 |
| 근거 생성 워크플로우 | 문서 인텔리전스; 분석 보조 | 데이터 계보 추적 + 감사 대응성 | 드리프트 미탐지 |
2. 산업 임팩트: 플랫폼, 데이터 자산, 협업 방식이 바뀐다
AI가 내재화되면서 전통적 제약사와 기술기업의 경계가 흐려진다. 대형 제약사는 AI 역량을 빠르게 확보하기 위해 파트너십·M&A를 확대하고, AI 네이티브 바이오텍은 플랫폼 기반으로 다수 파이프라인을 병렬로 운영하며 수익화한다. 조직 내부에서는 데이터가 자산으로 취급되기 시작했고, 거버넌스·계보·상호운용성이 실험 처리량만큼 중요해졌다.
CRO 관점에서 스폰서가 기대하는 것은 ‘툴 접근’이 아니라 ‘운영 통합’이다. 즉 SOP 정렬, 감사 대응 문서화, 검증된 분석, 벤더·기관·데이터 소유자 간 책임 구조를 한 번에 설계하는 역량이 중요해진다.
| 모델 | 적합 조건 | 장점 | 관리해야 할 위험 |
| Build(내재화) | 핵심 IP / 장기 차별화 | 통제력 극대화 | 인재·시간 투자 부담 |
| Buy(플랫폼 도입) | 표준화 가능한 업무 | 빠른 도입 | 투명성 부족 / 락인 |
| Partner(협업) | 도메인+현장 실행이 모두 필요 | 리스크 분담 + 속도 | 거버넌스 불명확 시 책임 공백 |
3. 규제 현실: 신뢰성과 라이프사이클 통제가 명시된다
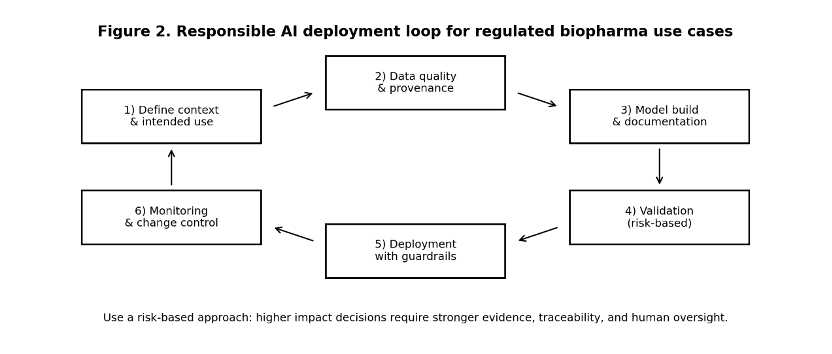
규제 환경에서 핵심 질문은 ‘정의된 사용 맥락(context of use)에서 해당 모델이 신뢰 가능한가’이다. 신뢰성은 홍보 문구가 아니라 증거로 입증해야 한다. 리스크 기반 검증, 문서화, 추적성, 라이프사이클 통제(버저닝·모니터링·변경관리)가 기본 요구로 자리 잡는 중이다.
모델이 환자 안전, 주요 엔드포인트, 또는 제출자료에 영향을 줄 수 있다면, 조직은 결과 재현성, 한계와 불확실성의 설명, 그리고 거버넌스(누가 검토했고 누가 승인했는지, 버전 간 무엇이 바뀌었는지)를 제시할 수 있어야 한다.
| 리스크 | 예시 | 필수 증거 패키지 | 거버넌스 |
| 낮음 | 작성/요약 생산성 도구 | 휴먼 리뷰 + 기본 정확도 점검 | 접근통제; 개인정보 유출 방지 |
| 중간 | 타당성/기관 스코어링 | 베이스라인 대비 벤치마크; 편향 점검 | 버저닝; 성능 모니터링 |
| 높음 | 제출자료 근거 생성에 영향 | 사용 맥락 검증; 추적성; 스트레스 테스트 | 변경관리; 독립적 리뷰 |
4. 임상 개발 접점
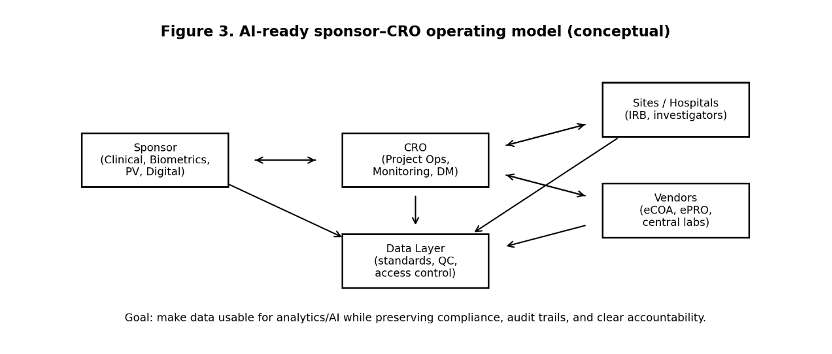
탐색과 근거 생성이 중심이어도, 임상 개발에서 AI 거버넌스는 현실이 된다. 대규모 데이터 기반 적격 환자 탐색, 분석 기반 모니터링, 참여자 지원 도구는 타임라인과 품질에 영향을 준다. 단, 데이터 보호와 책임 구조를 사전에 설계하지 않으면 리스크가 더 커진다.

5. 2026년 스폰서–CRO 실행
- 사용 맥락(COU)을 문장으로 정의한다: 모델이 맞으면 어떤 의사결정이 바뀌며 허용 오차는 무엇인가.
- 데이터 레이어를 먼저 만든다: 표준, QC, 계보, 접근권한, 감사 추적을 설계한다.
- 리스크에 맞춰 검증한다: 임팩트에 따라 증거 강도를 조정한다(표 3).
- 먼 오버사이트를 설계한다: 승인자, 오버라이드 권한자, 기록 책임자를 정한다.
- RO와 운영으로 내린다: SOP, 벤더 관리, 모니터링, 리포팅에 거버넌스를 내재화한다.
- 변경을 관리한다: 드리프트 탐지, 재검증 트리거, 버전 추적성을 유지한다.
FAQ
Q1. 바이오·제약 조직에서 가장 빠른 AI 첫 성과는 무엇인가?
A2. 데이터가 풍부한 병목(타겟 트리아지 또는 히트 엔리치먼트 등) 하나를 선택하고, 실험 검증 루프를 촘촘히 설계하는 것이 가장 빠르다.
Q2. 규제 환경에서 AI는 어떻게 접근해야 하는가?
A2. 사용 맥락을 먼저 정의하고, 리스크 기반 신뢰성 패키지(검증·문서화·추적성·라이프사이클 통제)를 준비해야 한다.
Q3. 규제·품질 관점에서 무엇을 문서화해야 하는가?
A3. 데이터 계보, 모델 버전, 검증 결과, 휴먼 오버사이트 규칙, 변경관리 트리거가 핵심이다.
Q4. AI 도입이 실패하는 대표 원인은 무엇인가?
A4. 데이터 품질과 일반화 실패이다. 기관 간 변동, 편향된 코호트, 배포 후 드리프트가 대표적이다.
Q5. CRO는 실행 외에 무엇을 더 할 수 있는가?
A5. QC 게이트, 감사 대응 기록, 역할·책임 정렬을 통해 거버넌스를 실제 운영으로 내릴 수 있다.
임상시험 수탁(CRO) 관련하여 보다 자세한 정보를 원하실 경우 BD Team전화(+82 02-515-8082) 혹은 이메일(bd@intoinworld.kr)로 통해 문의하시기 바랍니다.



