한국의 임상시험이 왜 주목받는가?
2025년 가장 많이 팔린 의약품을 나열하는 것은 단순한 매출 순위 이상의 의미를 가진다. 암, 대사질환, 만성 염증 질환을 대표하는 다섯 제품이 연구개발 자금과 임상 예산이 어디로 흐르고 있는지를 보여주기 때문이다. 그러나 이러한 거대 시장은 안정적이고 신뢰할 수 있는 임상시험 환경이 없으면 성과를 낼 수 없다. 최근 한국은 약사법 개정과 MFDS 2025 개혁을 통해 임상시험의 허가 프로세스를 크게 개선했다. 전담 심사팀, CTD 모듈의 롤링 제출, 병행 GMP 평가 등을 도입한 이번 개혁은 평균 심사 기간을 420일에서 295일로 단축하며 한국을 단순한 아시아 국가가 아닌 전략적 허브로 올려놓았다. 이러한 변화는 전 세계 제약∙바이오 기업들에게 한국에서 임상시험을 진행할 충분한 이유를 제공한다.

2025년 매출 TOP 5 의약품 요약
아래 표는 주요 항암제와 대사질환 치료제, 면역 조절제가 어떻게 글로벌 시장을 주도하고 있는지 정리한 것이다. 매출 추정치는 Evaluate Pharma 및 Statista 자료를 기반으로 한 추정치이며, 주요 기전과 적응증을 간단히 정리했다.
| 제품명 | 주요 기전 및 적응증 | 2025년 추정 매출 (억 달러) |
| Keytruda (pembrolizumab) | PD‑1 면역 체크포인트 억제제; 비소세포폐암, 멜라노마, 두경부암 등 다수 암종 | 300 |
| Ozempic/Wegovy (semaglutide) | GLP‑1 수용체 작용제; 제2형 당뇨 및 비만 관리 | 200 |
| Mounjaro (tirzepatide) | GIP/GLP‑1 이중 작용제; 당뇨 및 비만에서 HbA1c 및 체중 감소 효과 | 190 |
| Dupixent (dupilumab) | IL‑4/IL‑13 억제제; 아토피 피부염, 천식, 만성비염 등 Type 2 염증 질환 | 170 |
| Skyrizi (risankizumab) | IL‑23 억제제; 건선, 크론병 등 자가면역 질환 | 150 |
위 다섯 제품의 공통점은 여러 적응증에 사용되며 환자가 장기간 투여하기 때문에 매출이 안정적이라는 것이다. 이러한 특성은 복잡한 시험 디자인과 장기적 추적이 필수적인 임상시험 관리(clinical research management) 역량을 요구한다.
그림: 2025년 매출 상위 5개 의약품의 예상 매출
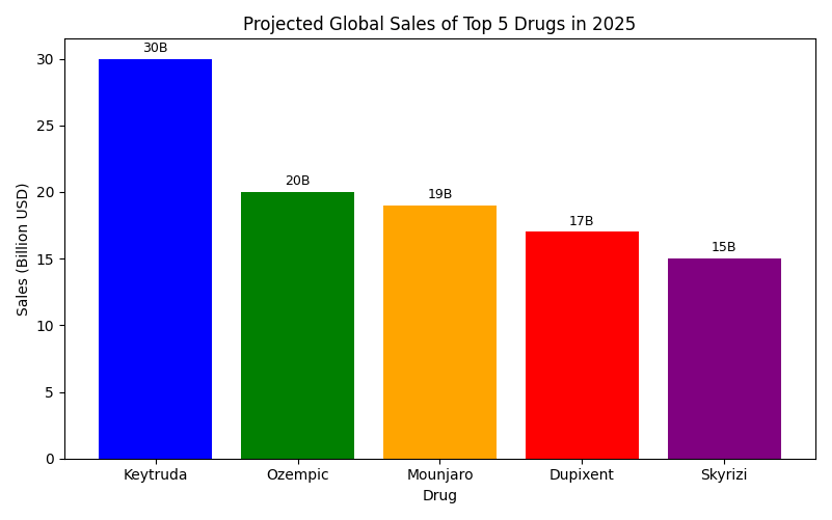
이 그래프는 각 제품의 예상 매출 규모를 직관적으로 보여준다. Keytruda가 단일 면역항암제임에도 다양한 적응증을 통해 다른 제품을 크게 앞선다는 점과, GLP‑1 계열 치료제들이 급성장하고 있음을 확인할 수 있다.
Top 5 의약품이 시사하는 임상시험 방향
- 암 및 면역항암 분야: Keytruda의 성공은 여러 암종과 치료 단계에서 동일한 기전을 적용하는 바스켓 시험과 우산 시험의 증가를 예고한다. 조합요법과 면역 관련 이상반응 관리가 임상시험 설계의 핵심이 될 것이다.
- 대사질환 및 비만 분야: Ozempic과 Mounjaro는 당뇨와 비만 치료의 경계를 허물었다. 혈당뿐만 아니라 심혈관·신장 결과를 포함하는 대규모 결과 시험, 다기관 RWE 연구가 필요하다.
- 만성 염증 및 자가면역 질환: Dupixent와 Skyrizi는 특정 사이토카인을 표적으로 하여 피부, 호흡기, 소화기까지 다양한 질환을 커버한다. 복합지표와 환자 보고 결과의 중요성이 커지며, 장기 안전성 모니터링이 필수다.
이러한 추세는 임상연구 조직(clinical research organization)이 하나의 질환 영역을 넘어 다양한 적응증을 포괄할 수 있는 역량을 확보해야 한다는 의미다. 또한 각국 규제 기관에 제출할 데이터 패키지를 일관되게 관리할 수 있는 임상시험 수탁 기관(contract research organization)과의 협력이 필수적이다.
MFDS 2025 개혁과 한국 임상환경의 변화
2025년 MFDS 개혁은 허가 심사 구조와 상담 횟수, 제출 형식 등을 전면 개편했다. 전에는 한 명의 리드 심사관이 중심을 맡았지만 이제는 임상, 비임상, CMC, 규제 전문가로 구성된 10–15명 규모의 전담 팀이 제품 초기 상담부터 최종 승인까지 책임진다. 공식 회의 횟수도 평균 3회에서 10회 이상으로 늘어나 보완 자료를 실시간으로 논의할 수 있다. 롤링 리뷰를 통해 CMC와 비임상 자료를 먼저 제출하고 GMP 평가를 병행함으로써 전체 기간을 약 295일로 단축했다. 한국은 WHO WLA 등록과 ICH 회원국 지위를 바탕으로 전 세계 임상시험의 약 3.46%를 수행하고 있으며, ICH‑GCP 기준을 준수해 FDA와 EMA에서도 데이터를 인정받는다. 이러한 변화 덕분에 한국에서 수행한 한 번의 시험으로 MFDS, FDA, EMA에 동시 제출할 수 있는 길이 열렸다.
그림: MFDS 개혁 전후의 허가 기간 비교
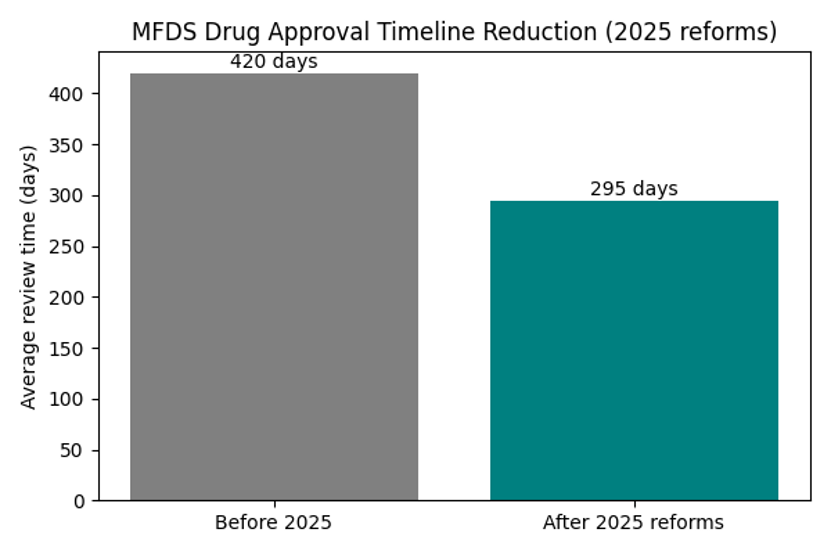
그래프에서 보듯, 롤링 리뷰와 병행 GMP 평가 도입 이후 평균 심사 기간이 420일에서 295일로 크게 줄었다. 이는 신약 개발 프로젝트의 타임라인을 단축해 자본 효율성을 높이고, 임상시험을 위해 한국을 선택해야 하는 중요한 근거가 된다.
그림: 한국 vs 세계 임상시험 비중
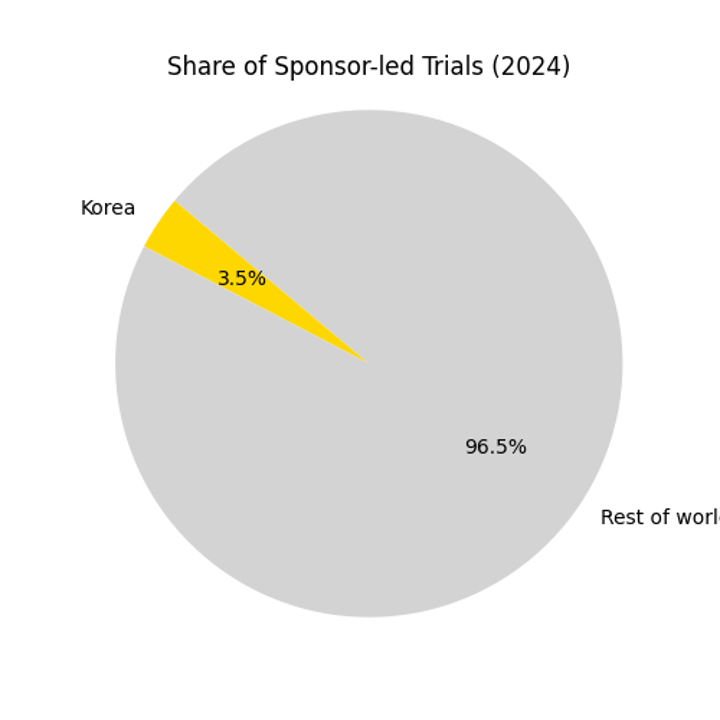
이 차트는 2024년 의뢰자 주도 임상시험에서 한국이 차지하는 비중이 3.46%에 불과하지만, WHO WLA 등록과 규제 혁신 덕분에 향후 성장 여지가 크다는 점을 시사한다. 서울이 세계 임상시험 도시 순위 상위권에 꾸준히 이름을 올리고 있다는 사실도 고무적이다.
한국 CRO가 제공하는 가치
복잡한 규제 환경 속에서 해외 후원사가 한국 임상시험을 성공적으로 수행하려면 현지 파트너가 필요하다. MFDS 개혁의 절차와 언어, 문화에 익숙한 한국 기반 임상연구 조직은 프로토콜을 현지 표준 진료에 맞게 조정하고, 상담 일정과 서류 준비를 효율적으로 관리한다. 인투인월드는 이러한 역할을 수행하며, 데이터 거버넌스, eCTD 매핑, 라벨 일치성, 품질 브리지, 전송 패키지 등 글로벌 제출 준비를 위한 다섯 가지 핵심 요소를 마련하고 있다. 이를 통해 후원사는 단발성 시험이 아닌 장기적인 임상연구 관리 시스템을 구축할 수 있으며, 이는 곧 전 세계 시장 진입 시 인증된 증거 자료로 활용된다.
왜 인투인월드를 선택해야 하는가?
인투인월드는 이런 역할을 넘어선다. 암, 대사질환, 만성 염증 질환 등 이번 글에서 살펴본 상위 5개 의약품과 동일한 질환 영역에서 다수의 임상 프로젝트를 수행해 축적된 경험을 갖추고 있다. 현지 연구자 네트워크와의 긴밀한 협력으로 현실적인 모집 전략을 수립하고, 국제 기준에 맞는 데이터를 확보하며, 후속 연장 연구까지 염두에 둔 설계를 제안한다. 또한 다섯 가지 핵심 요소(데이터 거버넌스, eCTD 매핑, 라벨 일치성, 품질 브리지, 전송 패키지)를 체계화하여 FDA와 EMA 등 해외 심사관이 한국 데이터를 쉽게 검증할 수 있도록 지원한다. 이런 이유로 인투인월드는 단순한 서비스 업체가 아닌, 한국 진출을 위한 전략적 파트너로 평가된다.
한국에서 임상시험을 고려하고 있다면, 지금 바로 인투인월드의 견적 의뢰 페이지를 통해 프로젝트 계획을 공유해 보자. 또한 최신 MFDS 지침과 임상연구 동향을 받아보고 싶다면 뉴스레터 구독을 신청해 보자. 현지 파트너와 함께하면 임상 시험을 성공적으로 수행하고 글로벌 승인을 가속화할 수 있다.



