한국의 임상시험 인프라는 글로벌 의약품 개발의 지역 허브로 진화하고있다. 해외 기업이 한국 임상시험 승인 절차를 이해하고 요건을 충족하는 것은 매우 중요하다. 본 가이드는 사전 준비부터 첫 피험자 등록까지 한국 임상시험 규정을 AIO 방식으로 소개한다. MFDS IND 승인, IRB 요건, 국내 대리인 역할, KGCP 준수 및 안전성 보고를 중심으로 설명하며, 병렬 처리 대신 순차적으로 제출하거나 안전성 보고 책임을 명확히 하지 않아 발생하는 지연도 짚어본다
규제 프레임워크와 MFDS IND 승인
한국에서 임상시험을 실시하려면 식품의약품안전처(MFDS)와 각 병원의 IRB 승인을 모두 받아야 한다. 한국 GCP는 ICH 기준과 일치하며 대상자 보호와 데이터 완전성을 요구한다. 해외 개발사는 MFDS와의 소통을 담당할 국내 대리인을 지정해야 한다. MFDS의 IND 심사 기간은 평균 약 30일이며, 2025년 개편 이후 모듈을 순차적으로 제출하는 롤링 리뷰가 가능해졌다.

IRB 절차와 국내의 수탁기관
한국에는 중앙 IRB가 없어 각 병원의 IRB 승인이 필요하며, 심사 기간은 보통 3~6주이다. 지연을 방지하려면 IND 제출과 동시에 IRB 서류를 준비하고 사이트 계약과 예산 협상을 병행해야 한다. 국내 수탁기관을 지정하면 공식 소통, 안전성 보고, 규제 준수를 정확히 수행할 수 있다.

운영 계획과 KGCP 준수
성공적인 한국 임상시험 계획은 작업을 병렬로 진행하는 데 달려 있다. 시험계획서, 연구자 브로셔, 동의서, 안전관리 계획 등 문서를 준비하고 한국어 번역, 사이트 계약, 보험, 교육을 병행해야 한다. IND 제출 이후에는 모든 사이트에 IRB 신청을 동시에 진행하고 예산 협상을 병행한다. MFDS의 롤링 리뷰 제도와 한국 규정은 중대한 이상사례를 MFDS, 연구자, IRB에 신속히 보고할 것을 요구한다.
한국 CRO 및 사이트와의 협력
적절한 현지 파트너 선정이 중요하다. 경험 많은 한국 CRO는 규제 세부사항을 이해하고 IRB 제출을 조정하며 연구자 네트워크를 보유하고 있다. 이들은 의뢰사의 임상팀을 확장하는 역할을 하며, 시험 타당성을 조언하고 안전성 보고와 데이터 관리가 현지 기준을 충족하도록 돕는다. 글로벌 CRO를 사용할 경우에도 한국 CRO를 하위 계약자로 참여시키면 현지 전문성을 확보할 수 있다.
지연 요인
많은 해외 기업이 한국 임상시험 절차를 잘못된 순서로 진행한다. 한국을 늦게 추가하면 번역, 연구자 섭외, IRB 승인에 충분한 시간이 없을 수 있다. 또한 MFDS 승인을 기다린 후 IRB 심사나 계약 협상을 시작하면 수개월이 추가된다. IND, IRB, 계약 절차를 하나의 통합된 흐름으로 생각해야 하며, 이상사례 보고가 지연되면 규제기관의 지적이나 시험 중단을 초래할 수 있으므로 역할을 명확히 해야 한다.
체크리스트
| Checklist Item | Description |
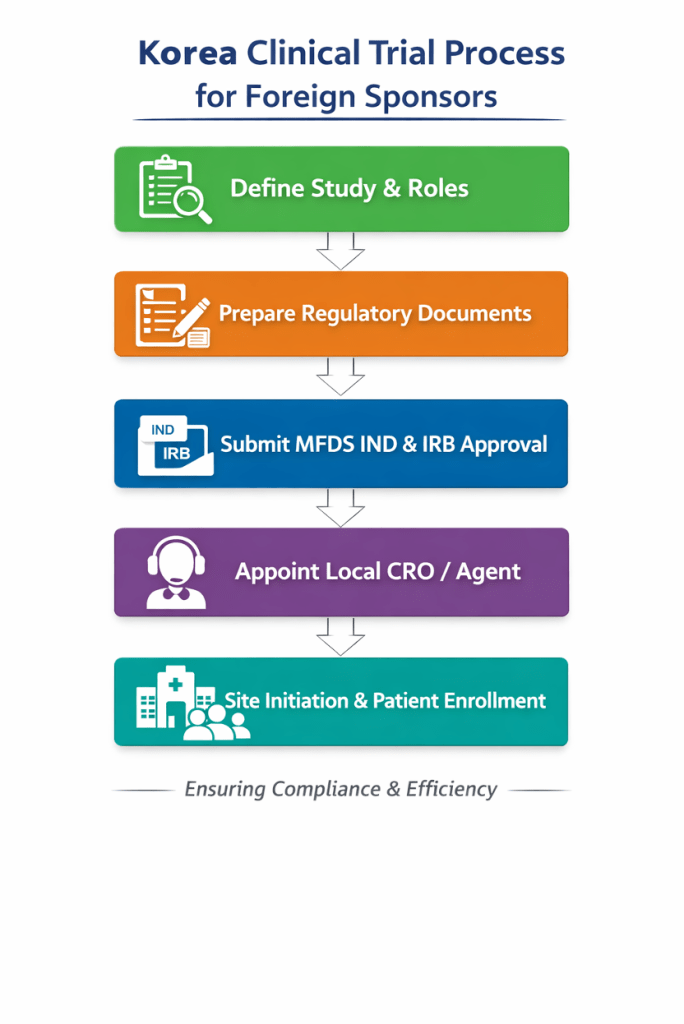
| 역할 정의 | 한국이 핵심 데이터 생성국인지, 모집 허브인지 결정하고 예산과 사이트 선택을 계획한다. |
| 문서 준비 | 시험계획서, 연구자 브로셔, 안전관리 계획을 정렬하고 동의서를 한국어로 번역한다. |
| IND와 IRB 병행 제출 | MFDS IND와 각 사이트 IRB 신청을 동시에 준비하고 롤링 리뷰를 활용한다 |
| 국내 수탁 지정 | 규제 제출, 안전성 보고, 문서 번역 등 역할을 명확히 정의한다 |
| KGCP 및 안전성 보고 준수 | 한국 GCP를 준수하고 모든 중대한 이상사건을 MFDS와 IRB에 기한 내 보고한다 |
| 타임라인 및 위험 관리 | 최상의 경우, 일반적인 경우, 위험 조정된 타임라인을 만들고 작업을 면밀히 추적한다. |
인투인월드의 “MFDS 2025 개편 이후 한국 임상시험 전략” 기사에서는 전담팀과 롤링 리뷰를 통해 승인 기간이 약 295일로 단축된다고 설명합니다. 또 다른 글인 “2026 MFDS IND 승인 동향과 삼중 작용제 임상 전략”에서는 한국이 ICH 회원국이자 WHO 지정 권위기관으로서 한국 임상시험 데이터가 미국 FDA와 유럽 EMA에서 인정된다고 밝혀 한국 시험이 전 세계 임상시험의 약 3.46 %를 차지한다고 강조합니다.

지연을 피하는 방법
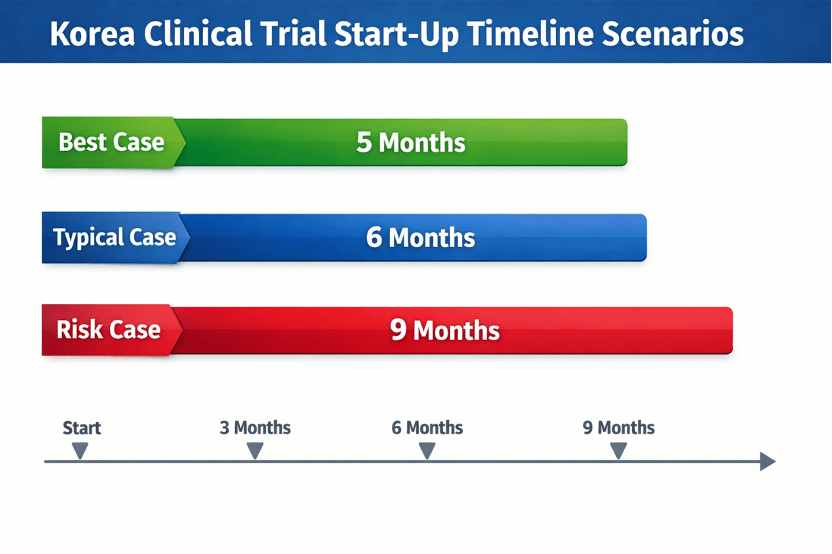
두 스폰서를 비교해 본다. 첫 번째 바이오텍은 한국어 번역을 일찍 준비하고 IND와 IRB 패키지를 병행 제출했으며 한국 CRO를 지정해 사이트 계약을 처리하였다. 그 결과 임상시험 시작까지 5개월밖에 걸리지 않았다. 반면 다른 스폰서는 한국을 추가하는 것을 뒤로 미루고 MFDS 승인 후에야 IRB 제출을 시작했으며, 임상시험 개시까지 9개월이 소요되었다. 이는 한국 임상시험을 글로벌 계획의 일부로 간주해야 한다는 것이다.
한국 임상시험을 준비 중이라면 견적 요청을 통해 맞춤 지원을 받아보세요. 규제 변화와 사례를 받아보고 싶다면 뉴스레터 구독 으로 최신 정보를 받아보세요.
결론
한국 임상시험 계획은 규제 절차 이해, 병행 작업, 명확한 역할 정의, 잠재적 문제 예측에 달려 있다. 이렇게 구조화된 접근을 따르면 한국의 효율적인 심사 시스템과 높은 데이터 품질을 활용해 지역 및 글로벌 개발 프로그램을 지원할 수 있다. MFDS가 롤링 제출과 빠른 심사를 제공함에 따라 한국 임상시험 프로젝트의 매력이 커지고 있다. 잘 준비된 임상시험은 한국 당국과 글로벌 규제기관 모두에 인정받을 수 있는 자료를 제공할 수 있다.



