식품의약품안전처(MFDS)는 한국의 신약 심사제도를 대대적으로 개편했다. 제품별 전담팀, 순차 제출, 병행 GMP 심사 등을 통해 신약 심사 기간을 약 420일에서 295일로 단축했다. 이러한 개편을 바탕으로 GIFT Korea, 우선심사, 조건부 허가라는 세 가지 패스트트랙 제도가 혁신 의약품의 허가를 더욱 앞당긴다. 이 글은 각 제도의 특징과 스폰서가 유의해야 할 전략을 설명한다.
패스트트랙 옵션 요약
| 경로 | 적용 기준 | 주요 혜택 |
| GIFT Korea | 생명을 위협하는 질환의 혁신적 의약품 | 조기 지정, 순차 심사, 심사 단계 단축; 일부 자료는 허가 후 제출 가능 |
| 우선심사 | 기존 치료 대비 임상적 개선 효과가 큰 치료제 | 심사 대기 순서 조정, 담당자와의 긴밀한 소통 |
| 조건부 허가 | 장기 데이터가 부족한 시급한 치료제 | 확증시험을 조건으로 조기 시판 허용 |
2025년 개편과 심사 일정
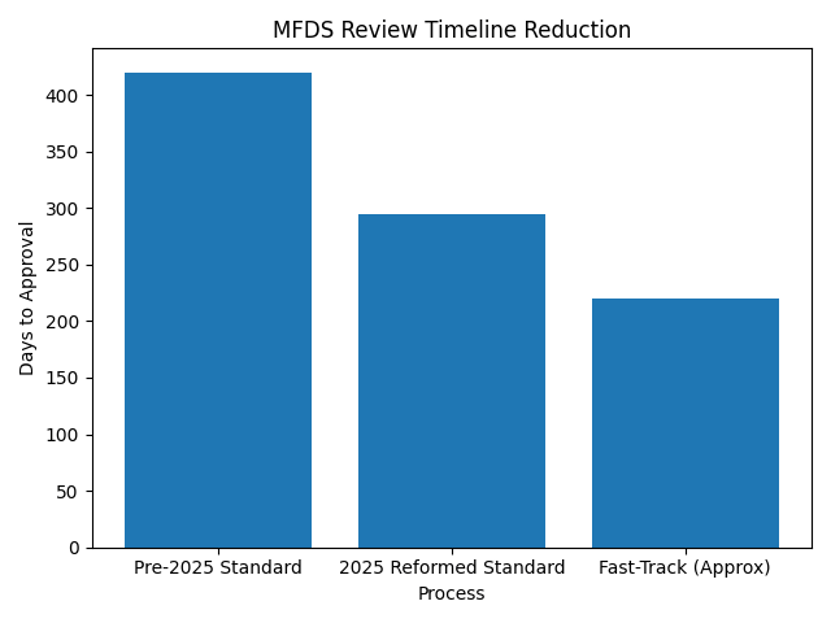
MFDS는 2025년 1월부터 새로운 심사 구조를 도입했다. 개발사는 최대 10회의 공식 미팅을 통해 MFDS와 소통할 수 있고, 제품별 전담팀이 신청부터 승인까지 일관되게 심사한다. 서류를 모듈별로 제출하는 순차 심사가 가능해졌고, GMP 실사는 기술 심사와 병행 진행된다. 이로 인해 평균 심사 기간이 약 295일로 단축되었으며, 패스트트랙 제도를 활용하면 이보다 더 빠른 승인이 가능하다.
그림 1: 심사 기간 단축
글로벌 인정 및 WLA 시대
한국은 WHO가 지정한 WLA(WHO‑Listed Authority) 중 하나이며, 2016년부터 ICH(국제의약품규제조화위원회) 정회원이다. 한국에서 수행되는 임상시험은 ICH‑GCP를 철저히 준수하고 미국 FDA와 유럽 EMA는 이러한 데이터를 공식적으로 인정한다. 즉, 한국에서 생성된 데이터는 미국과 유럽의 허가 심사에 직접 활용될 수 있고, 단일 임상시험으로 한국과 해외 승인 절차를 동시에 추진할 수 있다.

승인받는 전략과 성공 사례
그림 2: 글로벌 임상시험에서 한국의 비중
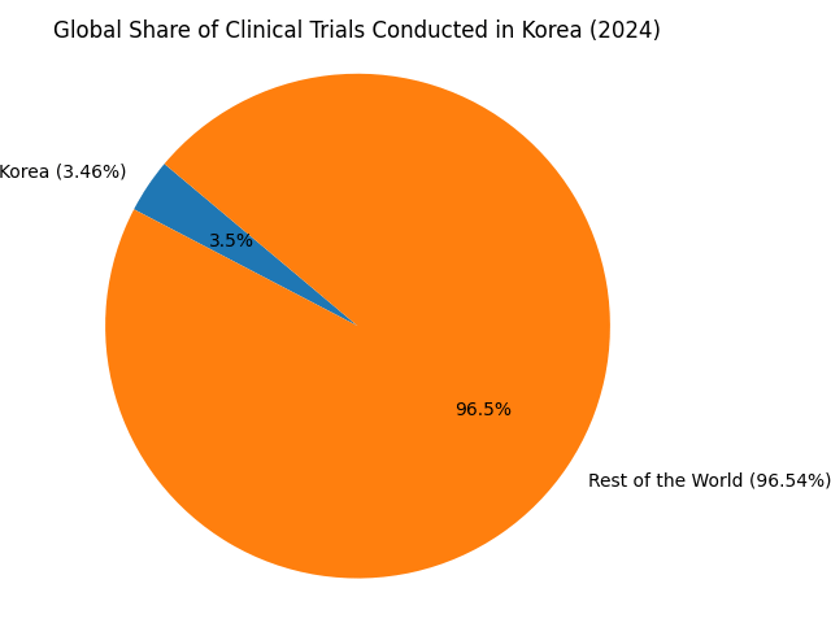
첨단 치료제를 위한 규제 혁신
이번 개편은 항체‑약물 접합체(ADC)와 3중 작용제 같은 혁신 기술에도 큰 영향을 미친다. 한국 기업은 글로벌 ADC 연구의 약 10%를 차지하고, 전담팀 확대와 순차 심사, 미팅 증가 등이 이러한 프로젝트를 가속화한다. 국내 CRO와 위탁제조사는 생산·임상 역량을 확장하며 첨단 치료제 개발을 지원한다.
개발사가 고려할 전략적 요소
- 적합성 평가: 제품이 한국 환자들의 미충족 의료 수요를 충족하는지 검토해야 한다. GIFT Korea나 우선심사를 받으려면 혁신성과 강력한 초기 데이터가 필요하다.
- 설계 정렬: 평가 변수와 비교군이 글로벌 요구사항과 한국 의료 관행에 맞도록 설계해야 한다. MFDS와 현지 연구자와의 조기 상담이 중요하다.
- 데이터 준비: 순차 심사를 활용하려면 임상·CMC 데이터 모듈을 빠르게 정리하여 제출할 수 있는 시스템이 필요하다.
- 진단 전략: 동반진단이 필요한 경우 환자군, 바이오마커 기준, 시험 플랫폼을 사전에 합의해야 한다.
- 현지 전문성 활용: 한국에 기반을 둔 CRO는 규제 요구사항과 언어·사이트 관리에서 중요한 파트너가 된다. 현지 파트너와의 협업은 성공적인 패스트트랙 신청에 도움이 된다.
자주 묻는 질문
Q1. 패스트트랙을 활용하면 안전성 기준이 낮아지나?
A: 아니다. GIFT Korea, 우선심사, 조건부 허가는 심사 일정만 단축할 뿐 안전성과 유효성 기준은 동일하게 적용된다.
Q2. 한 제품이 GIFT와 조건부 허가를 동시에 받을 수 있나?
A: 가능하다. GIFT는 심사 과정을 가속하고, 조건부 허가는 확증시험을 조건으로 조기 시판을 허용한다. 혁신적 치료제라면 두 제도를 함께 적용할 수 있다.
Q3. MFDS와 패스트트랙 논의는 언제 시작해야 하나?
A: 임상 개발 초기부터 MFDS에 문의해 패스트트랙 요건을 검토해야 한다. 초기 설계 단계에서 논의하면 한국 참여 비율, 평가 변수, 데이터 제출 계획을 효과적으로 조정할 수 있다.
한국에서 신약 개발을 가속화하고 싶다면 견적 의뢰하기를 통해 프로젝트 상담을 요청하거나, MFDS 동향과 임상시험 정보를 정기적으로 받아보고 싶다면 뉴스레터 구독하기를 누르면 된다.
식품의약품안전처(MFDS)는 한국의 신약 심사제도를 대대적으로 개편했다. 제품별 전담팀, 순차 제출, 병행 GMP 심사 등을 통해 신약 심사 기간을 약 420일에서 295일로 단축했다. 이러한 개편을 바탕으로 GIFT Korea, 우선심사, 조건부 허가라는 세 가지 패스트트랙 제도가 혁신 의약품의 허가를 더욱 앞당긴다. 이 글은 각 제도의 특징과 스폰서가 유의해야 할 전략을 설명한다.



